- Administración de Parques Nacionales. Sistema de Información de Biodiversidad. Argentina. (s.f.) Ficha: Chrysolampis mosquitus . Recuperado de https://sib.gob.ar/especies/Chrysolampis-mosquitus el 19/01/2020.
- Alves Pereira, G. & Severino Mendes de Azevedo Júnior (2013) Variaçao sazonal de aves em uma área de caatinga no nordeste do Brasil.Ornitología Neotropical; 24: 387–399 (enlace)
- ArgentAvis. (s.f.) Picaflor Pecho Naranja (Chrysolampis mosquitus) Recuperado de V el 19/01/2020.
- Barnett J.M., & Pearman, M. (2001) Lista Comentada de las Aves Argentinas. Editorial Lynx, Barcelona: 92 y 117
- BirdLife International (2018) Species factsheet: Chrysolampis mosquitus. Downloaded from http://www.birdlife.org on 12/12/2018.
- Braun, M.J. & Wolf, D.E. (1987) Recent records of vagrant South American land birds in Panama. Bull. Brit. Orn. Club 107(2): 115–117. (enlace)
- Chébez J.C., Castillo R. & Güller R.M. (2004) Notas sobre picaflores del noreste argentino. Hornero 19(1):1–5, 2004 (enlace)
- Correia Leal F., Lopes, A.V. & Machado, I.C. (2006) Polinização por beija-flores em uma área de caatinga no Município de Floresta, Pernambuco, Nordeste do Brasil. Revista Brasil. Bot., V.29, n.3, p.379-389 (enlace)
- Crease, A. (2009) Avian range extensions from the southern headwaters of the río Caroní, Gran Sabana, Bolívar, Venezuela. Cotinga 31: 5–19. (enlace)
- De la Peña, M.R. (2013) Citas, observaciones y distribución de aves argentinas: Edición ampliada. Serie Naturaleza, Conservación y Sociedad N° 7, Ediciones Biológica: 303
- De la Peña, M.R. (2015). Aves Argentinas. Buenos Aires EUDEBA, Vol.1: 347
- De la Peña, M.R. & Salvador, S. (2016) Aves Argentinas: Descripción, comportamiento, Reproducción y Distribución. Charadriidae a Trochilidae. Comunicaciones del Museo Provincial de Ciencias Naturales “Florentino Ameghino” (Nueva Serie); Vol.20 (1): 509-510
- EcoRegistros. (2020) Picaflor Topacio (Chrysolampis mosquitus) (Linnaeus, 1758). Recuperado de http://www.ecoregistros.org/ficha/Chrysolampis-mosquitus el 19/01/2020.
- Enciclopedia Británica (1998). Vol 15; Macropedia: Birds: 1-108
- Friedmann, H. & Smith, F.D. (1950) A contribution to the ornithology of northeastern Venezuela. Proc. US Natl. Mus. 100: 411–538. (enlace)
- Guilherme, E. & Dantas, S.M. (2011) Avifauna of the upper Purus River, state of Acre, Brazil. Rev. Bras. (enlace)
- Junge, G.C.A. & Mees, G.F. (1958) The avifauna of Trinidad and Tobago. Zool. Verhand. 37: 1–172. (enlace)
- Justino, D.G., Maruyama, P.K. & Oliveira, P.E. (2012) Floral resource availability and hummingbird territorial behaviour on a Neotropical savanna shrub. J. Orn.153(1): 189–197. (enlace idioma alemán)
- Las-Casas, F.M.G., Azevedo Júnior, S.M. & Dias Filho, M.M. (2012) The community of hummingbirds (Aves: Trochilidae) and the assemblage of flowers in a Caatinga vegetation. Braz. J. Biol. 72(1): 51–58. (enlace)
- Lepage, D. (2003). Avibase-La base de datos World Bird; Colibrí Rubí (Chrysolampis mosquitus) (Linnaeus, 1758). Recuperado de https://avibase.bsc-eoc.org/species.jsp?lang=ES&avibaseid=0ED012F9F8E9BA80 el 19/01/2020
- López-Lanús, B., P. Grilli, E. Coconier, A. Di Giacomo & R. Banchs (2008) Categorización de las aves de la Argentina según su estado de conservación. Informe de Aves Argentinas /AOP y Secretaría de Ambiente y Desarrollo Sustentable. Buenos Aires, Argentina.
- Machado, C.G., Coelho, A.G., Santana, C.S. & Rodrigues, M. (2007) Beija-flores e seus recursos florais em uma área de campo rupestre da Chapada Diamantina, Bahia. Rev. Bras. Orn. 15(2): 267–279. (enlace)
- Mallet-Rodrigues, F. (2007) Táxons de aves de validade questionável com ocorrência no Brasil. IV: Trochilidae (II). Atualidades Orn. 137: 18–20. (enlace)
- Narosky, T. & Yzurieta, D. (2010) Guía de identificación Aves de Argentina y Uruguay. Buenos Aires; Vázquez Mazzini Editores: 202
- Planqué, R., Vellinga, W.P., Pieterse, S., Jongsma J. & de By, R. (Xeno-canto Foundation). Colibrí rubí · Chrysolampis mosquitus · (Linnaeus, 1758). Recuperado de https://www.xeno-canto.org/species/Chrysolampis-mosquitus el 19/01/2020.
- Poulin, B., Lefebvre, G. & McNeil, R. (1994) Diets of land birds from northeastern Venezuela. Condor 96(2): 354–367. (enlace)
- Pugnali, G.D. & Pearman, M. (2001) Confirmación de la presencia del Colibrí Rubí (Chrysolampis mosquitus) en Argentina. Hornero 016 (02) : 093-095. www.digital.bl.fcen.uba.ar. Puesto en linea por la Biblioteca Digital de la Facultad de Ciencias Exactas y Naturales. Universidad de Buenos Aires (enlace)
- Raw, A. (1996) Territories of the Ruby Topaz hummingbird, Chrysolampis mosquitus, at flowers of the “Turk’s-cap” cactus, Melocactus salvadorensis in the dry caatinga of north-eastern Brazil. Rev. Bras. Biol. 56(4): 581–584. (enlace)
- Ruby-topaz Hummingbird (Chrysolampis mosquitus), In Neotropical Birds Online (T. S. Schulenberg, Editor). Cornell Lab of Ornithology, Ithaca, NY, USA. retrieved from Neotropical Birds Online: https://neotropical.birds.cornell.edu/Species-Account/nb/species/ruthum1
- Scherer-Neto, P., & Straube, F.C. (1995). Aves do Paraná: história, lista anotada e bibliografia. Curitiba: Ed. dos autores. (enlace)
- Schuchmann, K.L. & Kirwan, G.M. (2020). Ruby-topaz Hummingbird (Chrysolampis mosquitus). In: del Hoyo, J., Elliott, A., Sargatal, J., Christie, D.A. & de Juana, E. (eds.). Handbook of the Birds of the World Alive. Lynx Edicions, Barcelona. (retrieved from https://www.hbw.com/node/55413 on 17 February 2020).
- Snow, D.W. & Snow, B.K. (1986) Feeding ecology of hummingbirds in the Serra do Mar, southeastern Brazil. Hornero 012 (04) : 286-296 (enlace)
- Stotz, D.F., Fitzpatrick, J.W., Parker, T.A. & Moskovits, D.K. (1996) Neotropical Birds, Ecology and Conservation. University of Chicago Press, Chicago & London: 178-179
- Tobias, J.A. & Seddon, N. (2007) Nine bird species new to Bolivia and notes on other significant records. Bull. Brit. Orn. Club 127(1): 49–84. (enlace)
-
-
Picaflor topacio | Conservación
ESTADO DE CONSERVACIÓN SEGÚN BIRDLIFE INTERNACIONAL: PREOCUPACIÓN MENOREspecie con rango extremadamente amplio, por lo tanto no se aproxima a los umbrales de Vulnerabilidad bajo criterio de tamaño del rango (extensión < 20.000 km² combinado con declinación o fluctuación del tamaño del rango, extensión/calidad del hábitat, o tamaño de la población y número pequeño de localizaciones o fragmentación severa). La tendencia de la población parece ser estable por lo que no alcanzan los umbrales de los criterios de tendencia de la población ( declinación > 30% en 10 años o 3 generaciones). El tamaño de la población es muy grande, y no alcanza los umbrales de Vulnerabilidad bajo el criterio de tamaño de la población (< 10.000 individuos maduros con una declinación continua estimada ( > 10% en 10 años o 3 generaciones, o con una estructura poblacional específica). Por estas razones la especie es considerada como: Preocupación menor
El tamaño de la población global no ha sido cuantificado, pero esta especie se describe como «poco común» (Stotz et al., 1996)
En Argentina:
AvA-SADS-IC: Insuficientemente conocida según AvA SAyDS 2008 (Aves Argentinas y Secretaría de Ambiente y Desarrollo Sustentable) López-Lanús, B., P. Grilli, E. Coconier, A. Di Giacomo y R. Banchs. Categorización de las aves de la Argentina según su estado de conservación. Informe de Aves Argentinas /AOP y Secretaría de Ambiente y Desarrollo Sustentable. Buenos Aires, Argentina 1 ed. AOP: Buenos Aires, Argentina
Res348 SA-IC: Insuficientemente Conocida según SAyDS Res 348 (Secretaría de Ambiente y Desarrollo Sustentable) Categorización de aves autóctonas de Argentina. Lista de aves no registradas, endémicas y exóticas de Argentina 2010
MADS-AA-NA(oc): No Amenazada (ocasional) según MADS&AA 2015 (Ministerio de Ambiente y Desarrollo Sustentable de la Nación y Aves Argentinas) Categorización de las Aves de la Argentina según su estado de conservación. Informe del Ministerio de Ambiente y Desarrollo Sustentable de la Nación y de Aves Argentinas. 146 p 2015
-
Picaflor topacio | Distribución
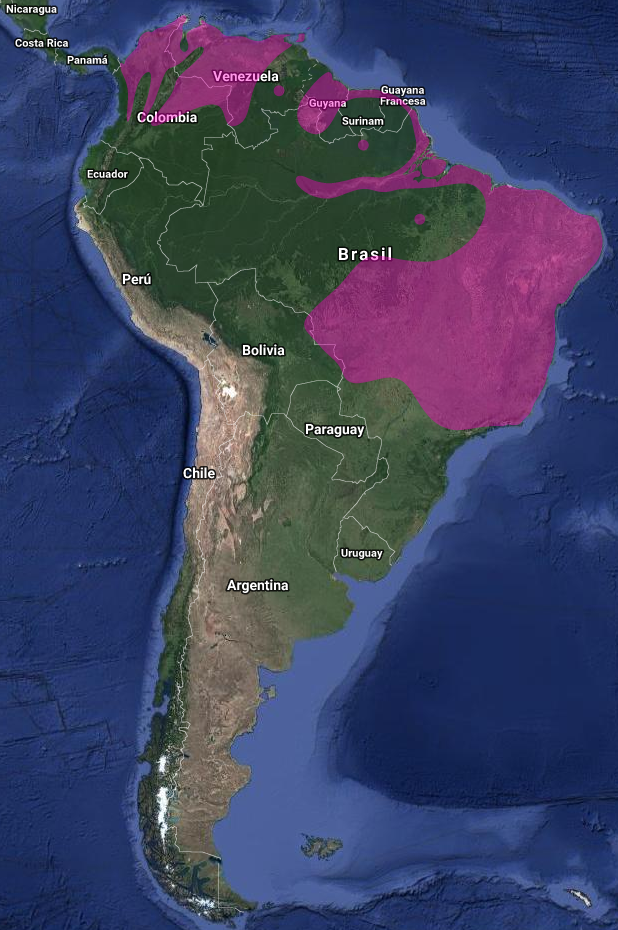
InfoNatura: Animals and Ecosystems of Latin America 2007 Su distribución geográfica un amplia área de Sudamérica que abarca desde el este de Panamá (Braun & Wolf, 1986), Colombia, Venezuela (Friedmann & Smith, 1950; Crease, 2009), las Guyanas; ocasionalmente avistado en noreste (Pernambuco) (Las-Casas, Azevedo Jr. & Dias Filho, 2012), centro y estado de Acre en Brasil (Guilherme & Dantas, 2011). En Brasil, Scherer Neto y Straube (1995) citan a la especie para Curitiba, Rolandia e Ilha do Mel, en el estado de Paraná, y Santa Catarina; Trinidad y Tobago (Junge & Mees, 1958); este de Bolivia (Tobías & Seddon, 2007), Paraguay y extremo noreste de Argentina.
En Argentina, Dabbene (1910) menciona que la especie fue obtenida en Misiones por Carlos Berg, sin mención de localidad, fecha u otro detalle (Barnett & Pearman, 2001). Esta cita es repetida por Chébez (1996), quien la registra entre las especies hipotéticas para Misiones. Observado en Puerto Iguazú, Misiones (Pugnali & Pearman, 2001; Chébez, Castillo & Güller, 2004; De la Peña, 2016)
Hábitat: se lo encuentra en vegetación similar a la sabana (incluyendo campos rupestres) y sus bordes desde el nivel del mar hasta las laderas áridas a 1300 msnm (Stotz et al., 1996), con migrantes registrados incluso en islas fluviales. Habita en bosques de galería, bosque deciduo tropical y estacionalmente en zonas bajas de pastos húmedos (Stotz et al., 1996)
Se alimenta desde niveles bajos hasta copas de árboles en claros, campo abierto, jardines y áreas cultivadas. Los más numerosos por debajo de los 500 msnm, aunque ocasionalmente de lo ha registrado a los 1750 msnm en Colombia (Stotz et al., 1996). Las aves en altitudes más altas actualmente no se están reproduciendo.
Ecorregiones: Selva Paranaense (Barnett y Pearman, 2001)
-
Picaflor topacio | Comportamiento
Migratorio estacional. Llega en mayo al sur del valle del Cauca, en Colombia, y desaparece en septiembre; ausente o raro en Trinidad y Tobago en agosto-noviembre y por el norte hacia Granada y quizás incluso a las Granadinas; aparece en Paraná, Brasil en octubre y parte de abril (donde ocasionalmente se registra en islas costeras); ha habido varios registros recientes (desde 2001) en noreste de Argentina (Misiones), y se considera únicamente un visitante de la estación húmeda (enero a mayo) en la Chapada Diamantina, Bahía (Brasil). Los registros recientes (documentados) del norte de Bolivia (en noviembre y abril) también sugieren la migración estacional, como respuesta a estacionalidad de recursos hídricos y tróficos asociados a las precipitaciones, durante la floración de semillas y frutos (Alves Pereira & Mendes de Azevedo, 2013)
VOCALIZACIONESCanto: serie de notas cortas de alta frecuencia, con timbre y cadencia de insecto ”trríí trríí trríí trríí”, entremezcladas con algunas notas más cortas.
ALIMENTACIÓNForrajea en el dosel (Stotz et al., 1996). Se alimenta de néctar de flores muy coloridas con aromas muy fuertes; también de árboles, arbustos, epífitas y cactus. Sin embargo prefieren las flores del Tamarindo (Samanea saman) e Ixora (Santa Rita, Coralillo y Cruz de Malta) dado que sus flores tienen un alto contenido de azúcar.
En un estudio sobre la polinización de los picaflores en la caatinga, en el Estado de Pernambuco, los autores (Correia Leal ,Lopes & Machado, 2006) citan como visitadas a las siguientes especies, Caesalpinia pyramidalis Tul. (Caesalpinaceae), Encholirium spectabile Mart. (Bromeliaceae), Ipomoea sp. (Convolvulaceae), Cnidoscolus cf. urens (L.) Arthur (Euphorbiaceae), Melochia tomentosa L. (Sterculiaceae) e Oxalis sp. (Oxalidaceae), todas en floración en la estación lluviosa, principalmente entre febrero y abril.
Ha sido observado alimentándose de las flores de Melocactus salvadorensis en la vegetación de la caatinga seca del noreste de Brasil (Raw, 1996)
Cuando se alimenta merodea hacia delante y atrás en el lugar; visita bebederos. También consume insectos y pequeños artrópodos, que captura en el aire o entre el follaje (Diptera, avispas, Araneae, Homoptera, Lepidoptera) (Poulin, Lefebvre & McNeil, 1994). Estos le proporcionan proteínas durante la época de reproducción (las hembras pueden capturar hasta 2.000 insectos al día mientras incuban) (Machado, Coelho, Santana & Rodrigues, 2007)
Las interacciones agresivas en flores que involucran al C. mosquitus se dirigieron principalmente a los conespecíficos, en lugar de a otras especies de colibríes. El macho defiende sus territorios de alimentación.
REPRODUCCIÓN
El periodo de reproducción depende del área de distribución; diciembre-junio en Trinidad y Tobago, Venezuela y Guayana; septiembre-enero en el resto. No forman pareja. Luego del cortejo y apareamiento, el macho deja a la hembra que se ocupará de construir el nido y criar a los pichones.
Nido sobre 1-4 m sobre el suelo construido con fibras vegetales suaves. Incubación de aproximadamente 16 días; puesta de 2 huevos blancos. Los pichones abandonan el nido entre los 19-22 días.
-
Picaflor topacio | Descripción
Dimorfismo sexual.
Pico corto, un poco más largo que la cabeza, recto, levemente curvado en la punta, de color negro.
Macho: Frente (alargada; las plumas crecen hacia delante del culmen, formando una extensión de plumas muy notable), corona y nuca rojo-rubí brillantes. Punto blanco post-ocular. Garganta y pecho dorado iridiscente (ocasionalmente verde-esmeralda). El pico es en promedio más largo que el del macho.
Dorso pardo oscuro con lustre oliva apagado. Vientre y subcaudales castaño-rojizas. Cola castaña-rojiza con las puntas negras que abre ampliamente al volar y alimentarse.
Hembra: Lados de la cabeza y zona ventral gris pálido. Dorso verde cobrizo claro.
Timoneras centrales verde oliva, las externas pardo-rojizas con banda amplia subterminal negra brillante y puntas blancas.

© Charles J. Sharp (diciembre 2014) Ruby-topaz hummingbird (Chrysolampis mosquitus) male in flight, Tobago. Algunos derechos reservados 
© Charles J. Sharp (diciembre 2014) Ruby-topaz hummingbird (Chrysolampis mosquitus) female, Tobago. Algunos derechos reservados -
Picaflor topacio | Taxonomía
Monotípico
Protónimo: «Trochilus mosquitus»
-
Picaflor topacio (Chrysolampis mosquitus)

Voegel aus Asien, Afrika, Amerika und Neuholland. Hahn, Carl Wilhem (1818-1822) Lámina III (Trochilus moschitus) El Picaflor topacio (Chrysolampis mosquitus) es una especie “poco común” que se distribuye geográficamente en el norte de Sudamérica, norte de la amazonia y Sudamérica central (Stotz et al., 1996). Habita regiones con vegetación de tipo sabana o arbustiva, en claros, zonas abiertas, jardines y áreas cultivadas, siendo una especie marcadamente migratoria.
NOMBRES COMUNES: Picaflor topacio (Argentina); Topacio rubí (Colombia y Panamá); Colibrí rubí (Paraguay); Tucusito rubí (Venezuela); Beija-flor-papo-de-fogo, Beija-flor-vermelhoen (Brasil); en guaraní: Mainumby, Mainumbý
EN OTROS IDIOMAS

BREVES APUNTES HISTÓRICOS
-
Méthode contenant la division des oiseaux en ordres, sections, genres, especes & leurs variétés. Brisson, Mathurin-Jacques, Martinet, François Nicolas. Parisiis :Ad Ripam Augustinorum, apud Cl. Joannem-Baptistam Bauche, bibliopolam, ad Insigne S. Genovesae, & S. Joannis in Deserto, 1760. Vol III: 699 y lámina XXXVII (Fig.1) (Oiseau mouche à gorge Topaze du Brésil)
- Planches enluminées d’histoire naturelle. Buffon J.L.Leclerc. [Paris] :[Imprimerie Royale] ;1770-1783. Vol I: Lámina 227 (Fig.2): (Oiseau-mouche à gorge dorée, du Brésil); Vol II: Lámina 640 (Fig.1) (Oiseau-mouche huppé à gorge topase de Cayenne)
- Oiseaux dorés ou à reflets métalliques. Audebert J.B, Vieillot L.P. A Paris :Chez Desray, libraire …,an XI—1802; Vol 1:124; Lámina 55 (Le rubis-topaze femelle)
- General zoology, or Systematic natural history. Shaw George. London,Printed for G. Kearsley, 1800-1826. Vol VIII (1812): pt 1-2: 323 (Amethystine Humming-bird/Trochilus amethystinus)
- Nouveau dictionnaire d’histoire naturelle, appliquée aux arts, à l’agriculture, à l’économie rurale et domestique, à la médecine, etc. Paris,Chez Deterville,1816-19. Vol VII (1817): 372 (L’oiseau-mouche rubis-topaze/Trochilus moschitus)
- Tableau encyclopédique et méthodique des trois règnes de la nature. Ornithologie. Bonnaterre, abbé (Pierre Joseph), Bénard, Robert, Vieillot, L. P. A Paris :Chez Mme. veuve Agasse …,1823. Vol II: 570 (L’oiseau-mouche améthyste)
- Histoire naturelle des oiseaux-mouches : ouvrage orné de planches dessinées et gravées par les meilleurs artistes … Lesson R.P. Paris :Arthus Bertrand,[1829-1830]. pp: 166 y láminas 52 y 53 (Le rubis-topaze/Ornismya moschita)
- A selection of the birds of Brazil and Mexico: the drawings. Swainson William. London :H.G. Bohn,1841; Lámina XXX (Trochilus moschitus)
- Voegel aus Asien, Afrika, Amerika und Neuholland. Hahn, Carl Wilhem, Kuster Heinrich Carl. Nurnberg :J.J. Lechner,1850. Vol I: Lámina III (Trochilus moschitus)
- A monograph of the Trochilidæ, or family of humming-birds. Gould John. London :Printed by Taylor and Francis ;1861 [i.e. 1849-1861]; Vol IV: Texto y lámina 204 (Chrysolampis moschitus)
- Conspectus generum avium. Bonaparte Charles Lucian. Lugduni Batavorum:Apud E.J. Brill,1850-1857. Vol I (1850): 82 (Trochilus moschitus)
- Trochilinarum enumeratio : ex affinitate naturali reciproca primum ducta provisoria. Reichenbach, H. G. Ludwig (Heinrich Gottlieb Ludwig). Lipsiae [i.e. Leipzig] :Friedericum Hofmeister,1855. Editio … secunda, emendata et aucta. Lámina DCCXXIII (Fig. 4646-9)
- An introduction to the Trochilidae, or family of humming-birds. Gould John. London :Taylor & Francis,1861; pp: 115 (Chrysolampis moschitus)
- Histoire naturelle des oiseaux-mouches, ou, Colibris constituant la famille des trochilidés. Mulsant M.E. Lyon :Au Bureau de la Société Linnéenne,1874-1877. Vol IV (1877): 210 (Chrysolampis moschitus)
- Catalogue of the Birds in the British Museum. British Museum (Natural History). Department of Zoology. [Birds]. London,1874-98. Vol 16: 113 (Chrysolampis mosquitus)
-
-
Picaflor amatista | Bibliografía
- Administración de Parques Nacionales. Sistema de Información de Biodiversidad. Argentina. (s.f.) Ficha: Calliphlox amethystina. Recuperado de https://sib.gob.ar/especies/Calliphlox-amethystina#_MISIONES el 19/01/2020
- Amethyst Woodstar (Calliphlox amethystina), In Neotropical Birds Online (T. S. Schulenberg, Editor). Cornell Lab of Ornithology, Ithaca, NY, USA. retrieved from Neotropical Birds Online: https://neotropical.birds.cornell.edu/Species-Account/nb/species/amewoo1
- Antunes, A.Z. (2003) Partilha de néctar de Eucalyptus spp., territorialidade e hierarquia de dominância em beija-flores (Aves: Trochilidae) no sudeste do Brasil. Ararajuba 11 (1): 39-44 (enlace)
- Argentavis. (s.f.) Picaflor amatista (Calliphlox amethystina) Recuperado de http://argentavis.org/2012/sitio/especie_co.php?id=663 el 19/01/2020
- Argentina nativa. (2011) Picaflor amatista (Calliphlox amethystina) Recuperado de http://faunayfloradelargentinanativa.blogspot.com/search?q=Calliphlox+amethystina el 19/01/2020.
- Barnett, J.M., & Pearman, M. (2001) Lista Comentada de las Aves Argentinas. Editorial Lynx, Barcelona: 51
- Belton, W. (1984) Birds of Rio Grande do Sul, Brazil. Part 1. Rheidae through Furnariidae. Bull. Amer. Mus. Nat. Hist. 178(4): 369–636. (enlace)
- Bertoni, A. de W. (1913) Contribución para un catálogo de aves argentinas. An. Soc. Cient. Arg. 75:64-102. (enlace)
- BirdLife International (2018) Species factsheet: Calliphlox amethystina. Downloaded from http://www.birdlife.org on 11/12/2018.
- Bodrati, A., Maders, C., Cockle, K., Pugnali, G. & Di Santo, G. (2008) El Picaflor Amatista (Calliphlox amethystina) en la Argentina. Nuestras Aves 53:39-41 (enlace)
- Bodrati, A., K. Cockle, J. M. Segovia, I. Roesler, J. I. Areta & E. Jordán. (2010) La avifauna del Parque Provincial Cruce Caballero, Provincia de Misiones, Argentina. Cotinga 32: 41-64. (enlace)
- Bond, J. & Meyer de Schauensee, R. (1943) The birds of Bolivia. Part II. Proc. Acad. Nat. Sci. Philadelphia 95: 167–221. (enlace)
- Castillo L., Güller R. & Veiga, J.O. (2012) Nuevo registro de Picaflor amatista (Calliphlox amethystina) para el norte de la provincia de Misiones, Argentina. Nótulas Faunísticas – Segunda serie, 88: 1-4 (enlace)
- Chébez, J.C. (1996). Fauna Misionera, Catálogo Sistemático y Zoogeográfico de los vertebrados de la Provincia de Misiones (Argentina) (1o Ed.). Monografía Nº 5; Editorial L.O.L.A. (Literature of Latin American): 137
- Chébez, J.C. (2008). Los que se van: Aves (1o ed.). Albatros: 287-290
- De la Peña, M.R. (2015). Aves Argentinas. Buenos Aires EUDEBA, Vol.1: 362
- De la Peña, M.R. (1999) Aves Argentinas. Lista y Distribución. Ed. L.O.L.A. Buenos Aires, Argentina: 101 (470)
- De la Peña, M.R (2013) Citas, observaciones y distribución de aves argentinas: Edición ampliada. Serie Naturaleza, Conservación y Sociedad N° 7, Ediciones Biológica, 786 pp.
- De la Peña, M.R. & Salvador, S. (2016) Aves Argentinas: Descripción, comportamiento, Reproducción y Distribución. Charadriidae a Trochilidae. Comunicaciones del Museo Provincial de Ciencias Naturales “Florentino Ameghino” (Nueva Serie); Vol.20 (1): 541-542
- EcoRegistros. Picaflor Amatista (Calliphlox amethystina) (Boddaert, 1783) Recuperado de http://www.ecoregistros.org/ficha/Calliphlox-amethystina el 19/01/2020.
- Enciclopedia Británica (1998). Vol 15; Macropedia: Birds: 1-108
- Gilliard, E.T. (1941) The birds of Mt. Auyan-Tepui, Venezuela. Bull. Amer. Mus. Nat. Hist. 77(9): 439–508. (enlace)
- Hayes, F.E. (1995) Status, Distribution and Biogeography of the Birds of Paraguay. Monographs in Field Ornithology 1. American Birding Association. Albany & Colorado Springs. 224 pp. (enlace)
- Hellmayr, C.E. (1929) A contribution to the ornithology of northeastern Brazil. Field Mus. Nat. Hist. (Zool. Ser.) 12(18): 235–501. (enlace)
- Herzog, S.K., Kessler, M., Maijer, S. & Hohnwald, S. (1997) Distributional notes on birds of Andean dry forests in Bolivia. Bull. Brit. Orn. Club 117(3): 223–235. (enlace)
- Justino, D.G., Maruyama, P.K. & Oliveira, P.E. (2012) Floral resource availability and hummingbird territorial behaviour on a Neotropical savanna shrub. J. Orn.153(1): 189–197. (enlace)
- Las-Casas F.M.G., Azevedo Jr., S.M. & Dias Filho, M.M. (2012) The community of hummingbirds (Aves: Trochilidae) and the assemblage of flowers in a Caatinga vegetation. Braz. J. Biol., vol. 72, no. 1, p. 51-58 (enlace)
- Lepage, D. (2003). Avibase-La base de datos World Bird; Colibrí Amatista (Calliphlox amethystina) (Boddaert, 1783). Recuperado de https://avibase.bsc-eoc.org/species.jsp?avibaseid=0431F843973D7B23 el 19/01/2020.
- López-Lanús, B., P. Grilli, E. Coconier, A. Di Giacomo & R. Banchs (2008) Categorización de las aves de la Argentina según su estado de conservación. Informe de Aves Argentinas /AOP y Secretaría de Ambiente y Desarrollo Sustentable. Buenos Aires, Argentina.
- Machado G.C., Góes Coelho A., Silveira Santana C. & Rodrigues M. (2007) Beija-flores e seus recursos florais em uma área de campo rupestre da Chapada Diamantina, Bahia. Revista Brasileira de Ornitologia 15 (2) 267-279 (enlace)
- Mobbs, A.J. (1975) The amethyst woodstar kummingbird, with observations on the eclipse plumage. The Avicultural magazine. Avicultural Society. Vol 81-82 (1975-1976): 13 (enlace)
- Narosky, T. & Yzurieta, D. (2010) Guía de identificación Aves de Argentina y Uruguay. Buenos Aires; Vázquez Mazzini Editores. pp: 207
- Olmos, F. & Boulhosa, R.L.P. (2000) A meeting of opportunists: birds and other visitors to Mabea fistulifera (Euphorbiaceae) inflorescences. Ararajuba 8(2): 93–98.(enlace)
- Partridge, W. H. (1954). Estudio preliminar sobre una colección de aves de Misiones. Rev. Mus. Arg. Cs. Nat. Zool. 3: 85-153.
- Planqué, R., Vellinga, W.P., Pieterse, S., Jongsma J. & de By, R. (Xeno-canto Foundation). Colibrí amatista · Calliphlox amethystina · (Boddaert, 1783). Recuperado de https://www.xeno-canto.org/species/Calliphlox-amethystina el 19/01/2020.
- Remsen, J.V. & Traylor, M.A. (1983) Additions to the avifauna of Bolivia, part 2. Condor 85(1): 95–98. (enlace)
- Renaudier, A. & Comité d’Homologation de Guyane (2010) Rare birds in French Guiana in 2005–07. Cotinga 32: 75–83. (enlace)
- Rojas, R. & Ribon, R. (1997) Guilda de aves em Bowdichia virgllioides(Fabaceae: Faboideae) em área de cerrado de Furnas, Minas Gerais. Ararajuba 5(2): 189–194. (enlace)
- Saibene C.A., Castelino M.A., Rey N.R, Herrera J., & Caló J. (1996) Inventario de las Aves del Parque Nacional «Iguazú», Misiones, Argentina. Ed. L.O.L.A. Monografía 9
- Sick Helmut. (1997) Ornitologia Brasileira. Editora Nova Fronteira, Rio de Janeiro: 464-465
- Stotz, D.F., Fitzpatrick, J.W., Parker, T.A. & Moskovits, D.K. (1996) Neotropical Birds, Ecology and Conservation. University of Chicago Press, Chicago & London: 186-187
- Zimmer, J.T. (1930) Birds of the Marshall Field Peruvian Expedition, 1922–1923.Field Mus. Nat. Hist. (Zool. Ser.) 17(7): 233–480. (enlace)
- Zimmer, J.T. (1953) Studies of Peruvian Birds. The genera Oreonympha, Schistes, Heliothryx, Loddigesia, Heliomaster, Rhodopis, Thaumastura, Calliphlox, Myrtis, Myrmia and Acestrura. Amer. Mus. Novit. 1604: 1-26 (enlace)
- Züchner, T. & Kirwan, G.M. (2018). Amatista Woodstar (Calliphlox amethystina). En: del Hoyo, J., Elliott, A., Sargatal, J., Christie, DA y de Juana, E. (eds.). Manual de los pájaros del mundo vivos. Lynx Edicions, Barcelona. (recuperado el 11 de diciembre de 2018).
-
Picaflor amatista | Conservación
ESTADO DE CONSERVACIÓN SEGÚN BIRDLIFE INTERNACIONAL: PREOCUPACIÓN MENOREspecie con rango extremadamente amplio, por lo tanto no se aproxima a los umbrales de Vulnerabilidad bajo criterio de tamaño del rango (extensión < 20.000 km² combinado con declinación o fluctuación del tamaño del rango, extensión/calidad del hábitat, o tamaño de la población y número pequeño de localizaciones o fragmentación severa). La tendencia de la población parece ser estable por lo que no alcanzan los umbrales de los criterios de tendencia de la población ( declinación > 30% en 10 años o 3 generaciones). El tamaño de la población es muy grande, y no alcanza los umbrales de Vulnerabilidad bajo el criterio de tamaño de la población (< 10.000 individuos maduros con una declinación continua estimada ( > 10% en 10 años o 3 generaciones, o con una estructura poblacional específica). Por estas razones la especie es considerada como: Preocupación menor
El tamaño de la población global no ha sido cuantificado, pero esta especie se describe como «poco común» (Stotz et al., 1996). Se sospecha que la población está en declive localmente por la pérdida de su hábitat (del Hoyo et al. 1999). Aparentemente más bien local en Colombia, donde no es muy conocido; Muy local en Venezuela, donde los registros se concentran en S del país.; poco común sobre E Perú; y también considerado como raro, aunque registrado regularmente, en la Guayana Francesa. Se extendió por gran parte de Brasil, pero el estado es poco conocido en el estado más al sur de Rio Grande do Sul, donde se registra principalmente en primavera y verano, y en un número relativamente pequeño de localidades. A lo largo de toda la gama parece aceptar hábitats artificiales como jardines y zonas verdes.
En Argentina: AMENAZADA
Según comenta Chébez (2008), las causas de su actual rareza no resultan demasiado claras. La fragmentación del hábitat con la consiguiente pérdida de determinadas plantas fanerógamas de cuyo néctar se alimenta podría llegar a ser una de las causas de su enrarecimiento y escasez.
Lugares donde se la ha encontrado (de acuerdo a las citas documentadas en el SIB): Misiones.
Los registros conocidos hasta el presente para la Argentina se produjeron entre los meses de octubre a abril (primavera-verano) etapa reproductiva de la especie (Castillo, et al., 2012)
Estado de conservación
AvA-SADS-AM: Amenazada según AvA SAyDS 2008 (Aves Argentinas y Secretaría de Ambiente y Desarrollo Sustentable) López-Lanús, B., P. Grilli, E. Coconier, A. Di Giacomo y R. Banchs. Categorización de las aves de la Argentina según su estado de conservación. Informe de Aves Argentinas /AOP y Secretaría de Ambiente y Desarrollo Sustentable. Buenos Aires, Argentina 1 ed. AOP: Buenos Aires, Argentina
MADS-AA-AM: Amenazada según MADS&AA 2015 (Ministerio de Ambiente y Desarrollo Sustentable de la Nación y Aves Argentinas) Categorización de las Aves de la Argentina según su estado de conservación. Informe del Ministerio de Ambiente y Desarrollo Sustentable de la Nación y de Aves Argentinas. 146 p 2015
Res 348 SA-A: Amenazada según SAyDS Res 348 (Secretaría de Ambiente y Desarrollo Sustentable) Categorización de aves autóctonas de Argentina. Lista de aves no registradas, endémicas y exóticas de Argentina 2010.
-
Picaflor amatista | Distribución
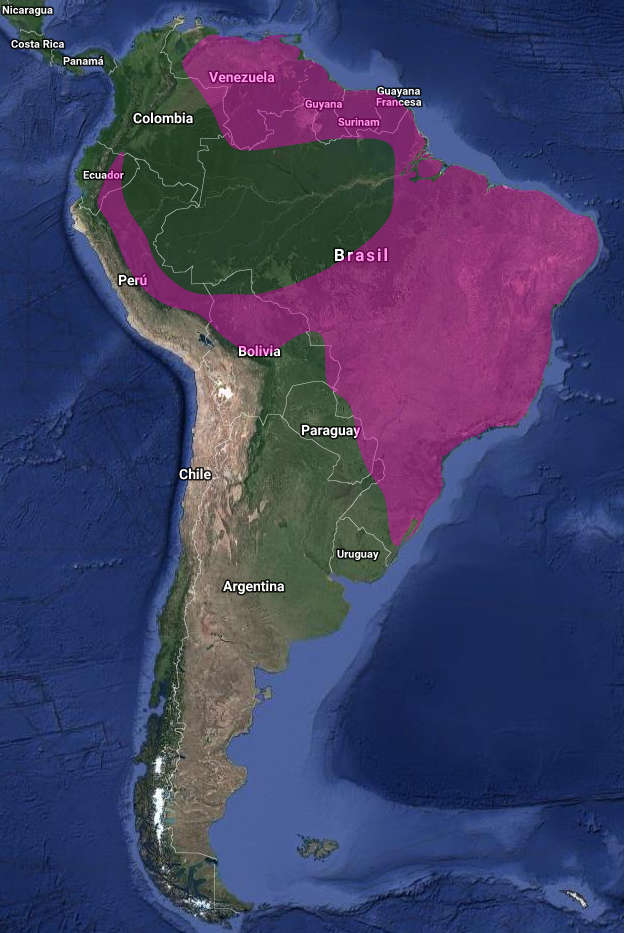
InfoNatura: Animals and Ecosystems of Latin America 2007 Sudamérica: Este de Colombia, Venezuela y las Guayanas, sur a este de Ecuador, este de Perú y norte de Bolivia, este de Brasil y por el sur hasta Paraguay y noreste de Argentina (Misiones) (De la Peña, 2016). Común en la mayor parte del rango; Aparentemente más bien local en este de Colombia, donde no es muy conocido. Muy local en Venezuela, donde los registros se concentran en el sur del país (Guilliard, 1941). Poco común en el este de Perú y Ecuador (Zimmer, 1953). También considerado como raro, aunque registrado regularmente, en la Guayana Francesa (Renaudier, 2009). En Bolivia muy raro con escasos registros (Remsen & Traylor, 1983; Herzog, Kessler, Maijer & Hohnwald, 1996). Se extiende por gran parte de Brasil; poco conocido en el estado más al sur de Rio Grande do Sul, donde la especie sería visitante estival (Belton, 1984; Saibene, Castelino, Rey, Herrera & Caló, 1996; Bodrati, Maders, Cockle & Pugnali, 2008), y en un número relativamente pequeño de localidades.
En Paraguay, Guyra Paraguay (2004) lo considera residente nidificante, pero Chebez y Rodríguez (2008) cuestionan esta designación, ya que no hay evidencia de su reproducción ni registros que demuestren su residencia a lo largo del año. Se lo considera raro en las regiones de Campos Cerrados, Centro de Paraguay y Alto Paraná (Hayes, 1995)
En Argentina: La especie fue incluida para la provincia de Misiones por Bertoni (1913); a posteriori Morgensen (1930) cita ejemplar recolectados en Bonpland (Dto Candelaria) y Puerto San Segundo (Dto Iguazú); según comenta Chébez (2008) es Partridge (1954) el que aporta nueva información en base a 5 ejemplares depositados en el MACN recogidos en la provincia de Misiones.
En el noreste de Argentina, la población parece haber disminuido y la especie se ha convertido en las más rara de los colibríes registrados regularmente en el Parque Nacional Iguazú (Castillo et al., 2012; Saibene et al, 1996)
Chébez (2008) comenta que en nuestro país posee un status raro, solo conocido por varios ejemplares colectados a principios y mediados del siglo XX, en la provincia de Misiones y un registro en el Parque Nacional Iguazú en enero de 1988 (Saibene et al., 1996), que ha sido puesto en duda aunque, en el año 2006, fue vuelto a observar en el área proyectada como Parque Provincial Caá-Yarí dentro de los límites de la Reserva Yabotí. Esto reconfirmaría su presencia en la provincia (Chebez, 2008)
Chebez (2008) la considera «en peligro» aunque considera que los datos son insuficientes.
Hay poca información sobre la presencia estacional de este picaflor en Argentina y zonas limítrofes. Narosky e Yzurieta (2003) lo consideran entre las especies que anidan en nuestro país y migran hacia el norte en invierno. En contraste, Mazar Barnett y Pearman (2001) no lo incluyen entre los migrantes.
Misiones (Bertoni 1913; De la Peña, 1999; De la Peña, 2013; De la Peña, 2016); citado para Parque Provincial Cruce caballero (Departamento de San Pedro) como raro, visitante estival de presencia indeterminada (Bodrati et al., 2010) y en el Parque Provincial Caá Yarí (Departamento de Guaraní (Chébez, 2008). Un registro en PN Iguazú en enero 1998 (Saibene et al., 1996), puesto en duda por Chébez (1998) y varios registros en 2011 en el Jardín de los Picaflores, en la ciudad de Puerto Iguazú (Bodrati et al., 2008; Castillo et al., 2012); Citada para los departamentos de Iguazú, San Pedro, Candelaria, General Belgrano y posiblemente Montecarlo (Bertoni, 1913; Partridge, 1954; Chebez, 1996; Chebez, 2008). (en Castillo y col. 2012). En determinadas regiones de Misiones se lo avista reiteradamente, lo cual podría indicar la tendencia de la especie a establecerse como posible residente y nidificante (Castillo et al., 2012)
Ecorregiones: Selva paranaense (Barnett & Pearman, 2001; Stotz et al, 1996; Chébez, 2008)
Hábitat: A lo largo de toda su distribución parece aceptar hábitats artificiales como jardines y zonas verdes, desde las fronteras de los bosques húmedos, los claros y las sabanas hasta los bosques abiertos (no está presente dentro de los bosques); Hasta 1500 msnm. Forrajea en arbustos y árboles bajos (Chébez, 2008)