- Administración de Parques Nacionales. Sistema de Información de Biodiversidad (SIB). Ficha Yeruvá (Baryphthengus ruficapillus); recuperado en diciembre 2025 de https://sib.gob.ar/especies/baryphthengus-ruficapillus?tab=avistajes
- Aleixo, A. & M. Galetti (1997). The conservation of the avifauna in a lowland Atlantic forest in south-east Brazil. Bird Conservation International, 7 (3): 235–261. (enlace)
- Anjos, L. & K. L. Schuchmann (1997). Biogeographical affinities of the avifauna of the Tibagi River Basin, Paraná drainage system, southern Brazil. Ecotrópica, 3 (1): 43–65. (enlace)
- Anjos, L., K. L. Schuchmann & R. Berndt (1997). Avifaunal composition, species richness, and status in the Tibagi River Basin, Paraná state, southern Brazil. Ornitología Neotropical, 8 (2): 145–173. (enlace)
- Alves, M. A. S., Ritter, P. D., Vecchi, M. B., Storni, A. & A. Bernades (1999). Feeding rates of Rufous-capped Motmot Baryphthengus ruficapillus nestlings in Atlantic Forest of Ilha Grande, RJ, Brazil. Ararajuba, 7 (1): 31-34. (enlace)
- Aleixo, A. (1997). Composition of mixed-species bird flocks and abundance of flocking species in a semideciduous forest of southeastern Brazil. Ararajuba, 5 (1): 11–18.
- Barnett, J. M. & M. Pearman (2001). Lista comentada de las aves argentinas. Lynx Edicions, Barcelona. 164 pp. ISBN 84-87334-32-6
- Belton, W. (1984). Birds of Rio Grande do Sul, Brazil. Part 1: Rheidae through Furnariidae. Bulletin of the American Museum of Natural History, 178 :369–636. (enlace)
- Bencke, G. A., G. N. Mauricio, P. F. Develey & J. M. Goerck, Editors (2006). Áreas Importantes para a Conservação das Aves no Brasil. Parte 1—Estados do Domínio da Mata Atlântica. SAVE Brasil, São Paulo, Brazil. (enlace)
- BirdLife International (2024). Species factsheet: Rufous-capped Motmot Baryphthengus ruficapillus. Downloaded from https://datazone.birdlife.org/species/factsheet/rufous-capped-motmot-baryphthengus-ruficapillus 21/12/2025
- Bodrati, A., K. Cockle, J. M. Segovia, I. Roesler, J. I. Areta & E. Jordan (2010). La avifauna del Parque Provincial Cruce Caballero, Provincia de Misiones, Argentina. Cotinga, 32: 41-64. (enlace)
- Bodrati, A., Areta J. I. & E. White (2012). La avifauna de la Posada y Reserva Puerto Bemberg, Misiones, Argentina. Nuestras Aves, 57: 63-80. (enlace)
- Capper, D. R., Esquivel, E. Z., Pople, R. G., Burfield, I. J., Clay, R. P., Kennedy, C. P. & J. Mazar (2000). Surveys and recommendations for the management of Aguará Ñu in the Reserva Natural del Bosque Mbaracayú, eastern Paraguay. (enlace)
- Chébez, J. C. (1995). Los manuscritos de William Henry Partridge. Nuestras aves, 32: 17-18. (enlace)
- Chébez, J. C. (1996:137). Fauna misionera, catálogo sistemático y zoogeográfico de los vertebrados de la provincia de Misiones (Argentina). Monografía Nº 5. L. O. L. A. Bs.Aires. 320 pp. ISBN 950-9725-20-X
- Chébez, J. C., N. R. Rey, M. Barbaskas & A. G. Di Giacomo (1998). Las Aves de los Parques Nacionales de la Argentina. Literature of Latin America, Buenos Aires, Argentina.
- Chébez, J. C. (2007). Parque Provincial Salta Encantado del Valle del Cuñá-Pirú. En Di Giacomo, A. S., M. V. De Francesco y E. G. Coconier (editores). 2007. Áreas importantes para la conservación de las aves en Argentina. Sitios prioritarios para la conservación de la biodiversidad: 303-304. Temas de Naturaleza y Conservación 5. CD-ROM. Edición Revisada y Corregida. Aves Argentinas/Asociación Ornitológica del Plata, Buenos Aires.
- de la Peña M. R. (1999). Aves Argentinas. Lista y Distribución. Ed. L.O.L.A. (Literature of Latin America). Monografía N.º 18; 244 pp. Buenos Aires. ISSN 0328-1620
- de la Peña, M. R. (2015). Aves Argentinas. Incluye nidos y huevos. 1º Ed. Santa Fe: Ediciones UNL; CABA: EUDEBA; Vol 1; 496 pp. ISBN 978-987-657-986-5
- de la Peña, M. R. (2016). Aves Argentinas: descripción, comportamiento, reproducción y distribución. Trogonidae a Furnariidae. Comunicaciones del Museo Provincial de Ciencias Naturales “Florentino Ameghino” (Nueva Serie), Vol. 20 (2): 1-620 ISSN 0325-3856
- de la Peña, M. R. (2020). Aves Argentinas. Descripción, Comportamiento, Reproducción y Distribución. (Actualización). Comunicaciones del Museo Provincial de Ciencias Naturales “Florentino Ameghino” (Nueva Serie), Vol 7: 1-344. ISSN 0325-3856
- del Hoyo, J. de. (2020). All the Birds of the World. Lynx Edicions, Barcelona. ISBN 978-84-16728-37-4
- eBird (2025). Ficha: Momoto yeruvá oriental (Baryphthengus ruficapillus); recuperado en diciembre 2025 de https://ebird.org/species/rucmot2/AR-N
- EcoRegistros (2025). Ficha: Yeruvá (Baryphthengus ruficapillus); recuperado en diciembre 2025 de https://www.ecoregistros.org/ficha/Baryphthengus-ruficapillus
- Giai, A. G. (1950). Notas de viajes. Por el norte occidental de Santa Fe y por el norte de Misiones. Hornero, 9 (2): 121-164. (enlace)
- Giraudo, A. R., Baldo, J. L. & R. R. Abramson (1993). Aves observadas en el sudeste, centro y este de Misiones (República Argentina), con la mención de especies nuevas o poco conocidas para la provincia. Nótulas Faunísticas, 49: 1-13. (enlace)
- Goerck, J. M. (1999). Distribution of birds along an elevational gradient in the Atlantic forest of Brazil: implications for the conservation of endemic and endangered species. Bird Conservation International, 9 (3): 235–253. (enlace)
- Guix, J. C. (1995). Aspectos da Frugivoria, Disseminação e Predação de Sementes por Vertebrados nas Florestas Nativas do Estado de São Paulo, Sudeste do Brasil. Ph.D. thesis, Universitat de Barcelona, Barcelona, Spain.
- Gwynne, J. A., R. S. Ridgely, G. Tudor & M. Argel (2010). Birds of Brazil: the Pantanal and Cerrado. Cornell University Press, Ithaca, NY, USA.
- Hayes, F. E. (1995). Status, Distribution and Biogeography of the birds of Paraguay. Monographs in Field Ornithology 1. American Birding Association, Colorado Springs, Colorado, USA. 224 pp. ISBN: 1-878788-30-2 (enlace)
- Krauczuk, E. R. (2008). Riqueza específica, abundancia y ambientes de las aves de Corpus Christi, San Ignacio, Misiones, Argentina. Lundiana, 9 (1): 21-31. (enlace)
- Lepage, D. (2003). Avibase-La base de datos World Bird. Ficha: Momoto Yeruvá Oriental (Baryphthengus ruficapillus -Vieillot, LJP 1818); recuperado en diciembre 2025 de https://avibase.bsc-eoc.org/species.jsp?avibaseid=C2966A667DC253F5
- Lowen, J. C., Clay, R. P., Brooks, T. M., Esquivel, E. Z., Bartrina, L., Barnes, R., Butchart, S. H. M. Y N. I. Etcheverry (1995). Bird conservation in the Paraguayan Atlantic forest. Cotinga, 4: 58–64. (enlace)
- Madroño, N. A., Clay, R. P., Robbins, M. B., Rice, N. H., Faucett, R. C. & J. C. Lowen (1997a). An avifaunal survey of the vanishing interior Atlantic forest of San Rafael National Park, Departments Itapúa/Caazapá, Paraguay. Cotinga, 7: 45-53. (enlace)
- Madroño, A., Robbins, M.B. & K. Zyskowski (1997b). Contribución al conocimiento ornitológico del Bosque Atlántico Interior del Paraguay: Parque Nacional Caaguazú, Caazapá. Cotinga, 7: 54–60. (enlace)
- Mallet-Rodrigues, F. & M. L. M. Noronha (2009). Birds in the Parque Estadual dos Três Picos, Rio de Janeiro state, south-east Brazil. Cotinga, 31: 96–107 (enlace)
- Martínez Gamba, R. (2014). Lista de aves del Parque Natural Municipal Monte Seguín, Provincia de Misiones, Argentina. Nótulas Faunísticas. Segunda Serie, 163: 1-10. (enlace)
- Narosky, T. & J. C. Chébez (2002). Aves de Iguazú: guía de identificación. 1º Ed. Vázquez Mazzini Editores, Buenos Aires. 128 pp. ISBN 987-9132-04-1
- Narosky, T. & D. Yzurieta (2010). Birds of Argentina and Uruguay: a field guide. Vázquez Mazzini Editores, Buenos Aires, Argentina. ISBN 950-99063-6-0
- Olivera, L. R. (2015). Reflejos en las aguas del moconá: naturaleza e historia del Parque Provincial Moconá, su entorno y su gente. 1º Ed. CABA: Fundación de Historia Natural Félix de Azara. 184 pp. ISBN 978-3781-13-1
- Parker, T. A. & J. M. Goerck (1997). The importance of national parks and biological reserves to bird conservation in the Atlantic Forest region of Brazil. In Studies in Neotropical Ornithology Honoring Ted Parker (J. V. Remsen, Editor). Ornithological Monographs, 48: 527–541. (enlace)
- Pereyra, J. A. (1950). Avifauna argentina (contribución a la ornitología). Hornero, 9 (2): 178–241. (enlace)
- Pimentel, L. & F. Olmos (2011). The birds of Reserva Ecológica Guapiaçu (REGUA), Rio de Janeiro, Brazil. Cotinga, 33: 6–22. (enlace)
- Planqué, R., Vellinga, W. P., Pieterse, S., Jongsma J. & R. de By. (Xeno-canto Foundation). Ficha: Momoto yeruvá oriental (Baryphthengus ruficapillus); recueprado en diciembre 2025 de https://xeno-canto.org/species/Baryphthengus-ruficapillus
- Protomastro, J. J. (2001). Nesting of Rufous-capped Motmot Baryphthengus ruficapillus in a tatu burrow. Cotinga, 15: 19-20.
- Ruschi, A. (1979). Aves do Brasil. Volume 1. Editora Rios, São Paulo, Brazil.
- Saibene, C. A., M. A. Castelino, N. R. Rey, J. Herrera & J. Calo (1996). Inventario de las Aves del Parque Nacional “Iguazú”, Misiones, Argentina. Literature of Latin America, Buenos Aires, Argentina.
- Schubart, O., A. C. Aguirre & H. Sick (1965). Contribuição para o conhecimento da alimentação das aves brasileiras. Arquivos de Zoologia do Estado de São Paulo, 12: 95–249.
- Sick, H. (1993). Birds in Brazil: A Natural History. Princeton University Press, Princeton, NJ, USA. ISBN 0-691-08569-2 (enlace)
- Sick, H. (1997). Ornitologia Brasileira. Editora Nova Fronteira, Rio de Janeiro, Brazil. 912 pp. ISBN 85-209-0816-0
- Silva, J. M. C., D. C. Oren, J. C. Roma & L. M. P. Henriques (1997). Composition and distribution patterns of the avifauna of an Amazon upland savanna, Amapá, Brazil. In Studies in Neotropical ornithology honoring Ted Parker. Ornithological Monographs ,48 (J. V. Remsen, Editor), American Ornithologists’ Union, Lawrence, KA, USA. pp. 743–762. (enlace)
- Silveira, L. F. (1998). The birds of Serra da Canastra National Park and adjacent areas, Minas Gerais, Brazil. Cotinga, 10: 55–63. (enlace)
- Snow, D. W. (2001). Family Momotidae (Motmotss). Pp. 264-284, en del Hoyo, J., Elliott A. & Sargatal, J. Eds.. Handbook of the Birds of the World. Vol. 6. Mousebirds to Hornbills. Lynx Edicions, Barcelona
- Snow, D. & G. M. Kirwan (2020). Rufous-capped Motmot (Baryphthengus ruficapillus), version 1.0. In Birds of the World (J. del Hoyo, A. Elliott, J. Sargatal, D. A. Christie, and E. de Juana, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.rucmot2.01
- Stotz, D. F., J. W. Fitzpatrick, T. A. Parker & D. K. Moskovits (1996). Neotropical Birds: Ecology and Conservation. University of Chicago Press, Chicago, IL, USA. 478 pp. ISBN 0-226-77629-8
- Straneck, R. (1990).Canto de las aves de Misiones. Buenos Aires, Argentina. (1º Ed.). L.O.L.A. (Literature of Latin America). Vol 1 y 2. ISBN 950-9725-05-06
- Straube, F.C. & M. R. Bornschein (1991). Revisão das subespecies de Baryphthengus ruficapillus (Coraciiformes: Momotidae). Ararajuba, 2: 65-67. (enlace)
- Willis, E. O. & Y. Oniki (1991). Avifaunal transects across the open zones of northern Minas Gerais, Brazil. Ararajuba, 2: 41–58. (enlace)
-
-
Yeruvá | Conservación
ESTADO DE CONSERVACIÓN SEGÚN BIRDLIFE INTERNACIONAL: PREOCUPACIÓN MENORDe acuerdo con Snow & Kirwan (2020), la especie no se encuentra globalmente amenazada. Aunque no existen estimaciones cuantitativas sobre el tamaño de su población, aparentemente no es poco común a escala local. No obstante, ha experimentado un declive generalizado como consecuencia de la deforestación y presenta registros escasos en el estado brasileño de Santa Catarina, a pesar de que allí la cobertura forestal se mantiene relativamente extensa (do Rosario, 1996, en Snow & Kirwan, 2020). La especie está presente en diversas áreas protegidas de Argentina, Paraguay y Brasil, donde ha sido registrada con distinta frecuencia, incluyendo el Parque Nacional de Iguazú y el Parque Provincial Urugua-í en Argentina; el Parque Nacional de San Rafael y el Parque Nacional de Caaguazú en Paraguay (Madroño et al., 1997a:52/Madroño et al., 1997b:57); así como numerosos parques nacionales, estatales y reservas biológicas en Brasil, entre ellos Serra da Canastra, Sooretama, Desengano, Serra dos Órgãos, Itatiaia, Serra do Mar, Serra do Tabuleiro y Turvo, entre otros (Silveira, 1998:7; Bencke et al., 2006:293/324/362/399/419/448; Mallet-Rodrigues & Noronha, 2009:104; Pimentel & Olmos, 2011:10; Snow & Kirwan, 2020).
(Birdlife International, 2024): Esta especie tiene un rango extremadamente grande y por lo tanto no se aproxima a los umbrales DE Vulnerabilidad bajo criterio de tamaño de la extensión de la población (Extensión < 20.000 km² combinado con una declinación o fluctuación del tamaño de la extensión, extensión/calidad del hábitat, o tamaño de la población y un pequeño número de localizaciones o con fragmentación grave). A pesar de que la población parece estar disminuyendo, no se cree que esta declinación sea suficientemente rápida como para acercarse a los umbrales de Vulnerabilidad bajo el criterio de tendencia poblacional (disminución > 30% en diez años o en tres generaciones). El tamaño de la población no se ha cuantificado, pero no se cree que se aproxime a los umbrales umbrales de Vulnerabilidad bajo el criterio de tamaño de la población (<10.000 individuos maduros con una disminución continua estimada > del 10% en diez años o en tres generaciones o con una estructura de población específica). Por estas razones, la especie es evaluada como de «preocupación menor».
No se ha cuantificado el tamaño de la población mundial, pero esta especie se describe como «común» (Stotz et al., 1996:190).En Argentina (Baryphthengus ruficapillus):
AvA-SADS-NA: No amenazada según AvA SAyDS 2008 (Aves Argentinas y Secretaría de Ambiente y Desarrollo Sustentable). López-Lanús, B., P. Grilli, E. Coconier, A. Di Giacomo y R. Banchs. Categorización de las aves de la Argentina según su estado de conservación. Informe de Aves Argentinas /AOP y Secretaría de Ambiente y Desarrollo Sustentable. Buenos Aires, Argentina 1º ed. AOP: Buenos Aires, Argentina
Res 348 SA-NA: No Amenazada según SAyDS Res 348 (Secretaría de Ambiente y Desarrollo Sustentable). Categorización de aves autóctonas de Argentina. Lista de aves no registradas, endémicas y exóticas de Argentina 2010. -
Yeruvá | Distribución
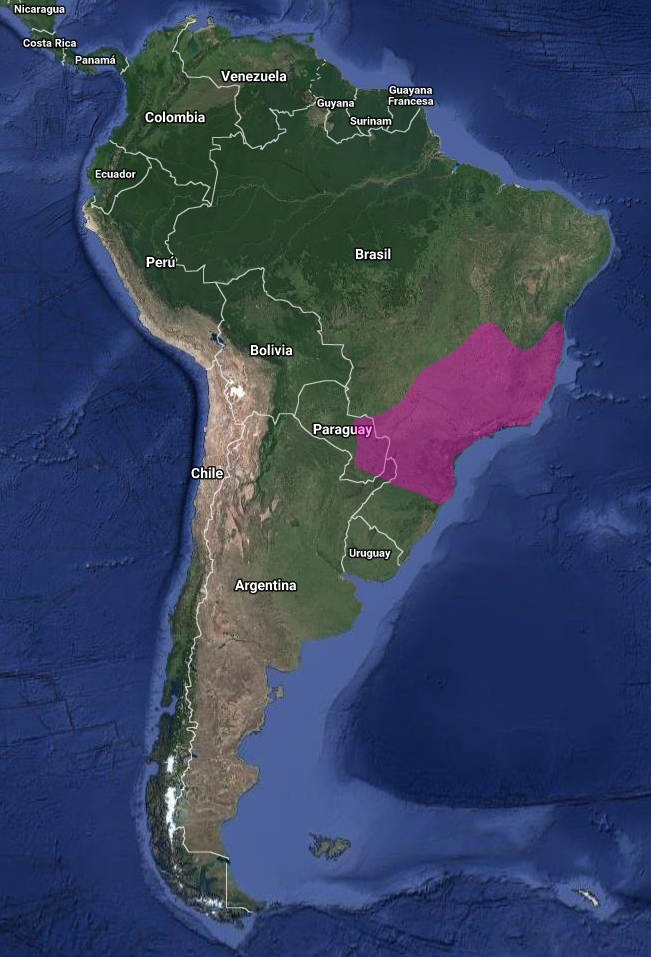
InfoNatura: Animals and Ecosystems of Latin America 2007 Se distribuye entre Este y Sur de Brasil (Bahía y Centro y Sur de Goiás hasta Mato Grosso do Sul y Norte de Rio Grande do Sul), Este de Paraguay y Noreste de Argentina (Misiones).
Distribución geográfica en Argentina (de la Peña, 2016:24; de la Peña, 2020:25)
Baryphthengus ruficapillus (Vieillot, 1818) en la provincia de Misiones.
Hábitat
Bosques bajos y de segundo crecimiento por talas; bosque de galería a lo largo de cursos de agua; hasta 1250 msnm (Stotz et al., 1996:190)Ecorregiones: Endémico de la Selva Paranaense (Barnett & Pearman, 2001:51; Stotz et al., 1996:190).
-
Yeruvá | Comportamiento
Es un ave de hábitos solitarios, comportamiento pasivo y actividad predominantemente crepuscular. Se desplaza principalmente en los estratos medios e inferiores de la selva paranaense, donde suele permanecer posada en posición vertical, balanceando lateralmente su larga cola péndula. La defensa del territorio se realiza mediante vocalizaciones graves y profundas. Por lo general solo o en parejas y se reproduce en taludes o bancos cercanos al nivel del suelo. Su vuelo es lento y ondulado, característica atribuida a la corta longitud de sus alas (Snow & Kirwan, 2020).
VOCALIZACIONESLa especie presenta una actividad vocal predominantemente crepuscular y nocturna, con mayor frecuencia antes del amanecer y al atardecer.
Sus vocalizaciones consisten en emisiones breves, guturales y de carácter profundo, transcripto fonéticamente como “bu.ru.bu.bup” o “jurrrr”, repetido de forma esporádica y con clara preferencia por las horas del crepúsculo (de la Peña, 2015:370; de la Peña, 2020:24; Straneck en de la Peña, 2016). Otros autores coinciden describiéndolas como burbujeos sonoros y graves, tales como “bubububububub” (Belton, 1984:583), o como llamados secos y ventrílocuos, incluyendo variantes como “búuuu”, “du-dúg-dug-dug-dug-dug” y “rrrrü” (Sick, 1997:477). Estas emisiones suelen ser más audibles en ambientes de selva densa y oscura, donde la especie habita preferentemente (Snow & Kirwan, 2020; de la Peña, 2020:24).ALIMENTACIÓNLa dieta de la especie se compone principalmente de insectos grandes y sus larvas, arañas, moluscos terrestres, pequeños reptiles, mamíferos y aves, con un aporte ocasional de fruta. En el caso de los jóvenes en el nido, su alimentación incluye artrópodos (41,8%), frutas (32,8%), gusanos (7,4%), pequeños vertebrados como ranas y lagartijas (6,6%), moluscos (0,8%) y elementos no identificados (10,6%). Dentro de los artrópodos, predominan los insectos (74,5%), seguidos por diplópodos, siendo los más comunes los Coleóptera (10%), Orthoptera, como los insectos palo (30%), Hymenoptera, especialmente hormigas y, en menor medida, abejas (60%), y orugas (30%). A medida que los jóvenes se desarrollan, la proporción de artrópodos disminuye, mientras que el consumo de frutos, especialmente de Virola gardineri y una especie de Myrtaceae, aumenta significativamente en la fase de volantón (Alves et al., 1999:33). Además, ocasionalmente sigue a las hormigas arrieras, aprovechando presas perturbadas por ellas, y a veces se une a bandadas mixtas de forrajeo (Aleixo, 1997, en Snow & Kirwan, 2020).
REPRODUCCIÓNSe caracteriza por anidar en madrigueras excavadas entre enero y abril, período en el que el suelo se mantiene húmedo debido a las lluvias estivales. La puesta ocurre probablemente entre septiembre y octubre, con registros de polluelos alimentados a comienzos de octubre y durante la segunda mitad de noviembre, así como de juveniles recién volantones a principios de diciembre (Alves et al., 1999:33). Asimismo, se ha documentado un nido activo, aunque sin huevos, en noviembre en el noreste de Argentina (Protomastro, 2001:19).
El nido consiste en una madriguera excavada en bancos de tierra o reutilizada a partir de cavidades abandonadas por otros animales, como armadillos (Tatú), cuya estructura puede diferir notablemente. Generalmente presenta un túnel de más de 1 m de longitud que culmina en una cámara sin revestimiento de aproximadamente 35 × 14 cm. En el Parque Nacional Iguazú (departamento Iguazú, Misiones), se describió un nido en el suelo con dos entradas de 10 a 12 cm de diámetro, una asociada a una antigua cueva de tatú; el túnel medía 2,8 m de longitud y la cámara terminal, ubicada a 25 cm de profundidad, presentaba dimensiones similares (de la Peña, 2016:24). Protomastro (2001:19) también describió un nido excavado en el techo de una gran cavidad posiblemente perteneciente a un tatú, con galerías inactivas cercanas correspondientes a ciclos reproductivos previos; la galería activa alcanzaba 2,8 m y poseía una segunda entrada situada a 0,8 m de la cámara, aparentemente utilizada exclusivamente para la atención del nido.
La puesta consta de dos a tres huevos y ambos sexos participan en la alimentación de las crías, con visitas al nido que oscilan entre 0 y 10 por hora; sin embargo, se ha observado que uno de los miembros de la pareja puede invertir más en el cuidado parental, mientras el otro compensa mediante una mayor dedicación a la defensa territorial y a comportamientos antidepredadores (Alves et al., 1999:33). Previo a ingresar a la madriguera, ambos adultos muestran un comportamiento cauteloso, posándose repetidamente en ramas cercanas e inspeccionando el entorno; durante este proceso, realizan movimientos pendulares de la cola, característicos de los momotos y particularmente intensos durante la época reproductiva (Alves et al., 1999:32–33).
A pesar de que se conoce que ambos miembros de la pareja reproductora excavan el túnel y nidifican en una cámara ubicada a lo largo de este, la información disponible sobre la ecología reproductiva de la especie sigue siendo limitada (Sick, 1997). Un diagrama detallado de la estructura del nido se presenta en Alves et al. (1999:32). -
Yeruvá | Descripción

© Francesco Veronesi. Animalia Bio. Rufous-capped Motmot – Intervales NP – Brazil. Algunos derechos reservados Según los siguientes autores: Belton, 1984:583; Sick, 1997:477; Snow, 2001:264;Snow & Kirwan, 2020; de la Peña, 2015:370; de la Peña, 2020:24.
Sexos similares.
Ambos sexos tienen la frente, corona y nuca castaño rojizas. Lores, plumas por encima del ojo (superciliares), lados de la cara y auriculares negras bordeados de turquesa.
Mejillas, garganta y parte superior del pecho color oliva-azulado.
Partes superiores verdes con reflejos amarillentos, volviéndose verde-oliva en espalda y lomo, incluidas las cubiertas alares y la cola. Cubiertas alares primarias y remeras verdes más azuladas-brillantes en las puntas.
Garganta y pecho verde oliva. En zona superior y central del pecho mechón de plumas elongadas de color negro con puntas verdes (a veces ausentes durante la muda). Banda en parte inferior del pecho rojo-canela y parte inferior del vientre y subcaudales verde azulado.
Vientre y subcaudales verde-azulado.
Cola larga verde con reflejos azulados.
Pico negro, aserrado; patas y pies gris oscuro/marrones-grisáceas claras.
Iris marrón-rojizo oscuro.
Juvenil más apagado que el adulto.
Se diferencia del B. martii totalmente alopátrico por un plumaje generalmente más verde y apagado, con menos rufo, cola más corta y marcadamente menos graduada, timoneras centrales que se estrechan hasta un extremo romo sin raquetas.
-
Yeruvá | Taxonomía

Monotípico.
Estrechamente relacionado con B.Martii, y a menudo tratado como con-espespecífico. En estudios recientes se ha demostrado que las razas propuestas: aeruginosos (Mina Gerais, Rio de Janeiro), septentrionalis (Sao Pablo) y abreui (Paraná) solo se basan en variaciones individuales, sin significación geográfica.
Se considera el nombre berlai (Goiás) como inválido (Snow & Kirwan, 2020). -
Yeruvá (Baryphthengus ruficapillus)

© La galerie des oiseaux. Vieillot, L. P., (1825). Vol II: Ilustración 190. (Le momot Dombey – Baryphonus ruficapillus) El Yeruvá (Baryphthengus ruficapillus), es una especie endémica de la Mata Atlántica, y anteriormente considerado congénere del Momoto Yerubá occidental (Baryphthengus martii) de la Amazonía occidental y Centroamérica. No obstante, se diferencia claramente por sus partes inferiores mayoritariamente verdosas, interrumpidas sólo por una banda rufa en la parte inferior del pecho; por la corona rufa bien definida, que no se extiende hasta la nuca; y por la ausencia de raquetas evidentes en la cola. La especie se distribuye desde el este de Brasil hasta el sur y este de Paraguay y el extremo noreste de Argentina, habitando bosques de tierras bajas y bosques secundarios de altura, al menos hasta los 1200 msnm (Snow & Kirwan, 2020).
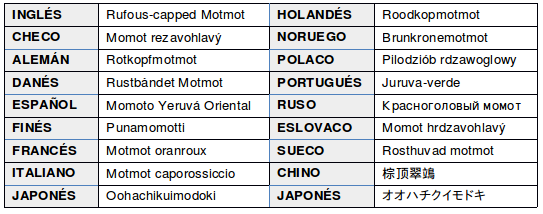
Nombres comunes: Yeruvá (Argentina, Bolivia y Paraguay); Taragón rojizo (Honduras); Burgo rojizo, Momoto yeruvá oriental; Jeruva, Juruva, Juruva-verde; (Brasil) Bururuk, (Botocudo), Jeruva, Pururu, Formigão (Bahía), Juruva-verde? En Goiás es simpátrico con Momotus momota (Burgo) (Sick, 1997:477); En guaraní: «Jiru, Marakana yvyguy», Yirú, marakaná-ihvihgwíh, guirá-hú-tacuara, güirá-payé, güirá-ivigüí, güirá-hú-ivigüí, yakú-tacuara o loro-ybuibui, yeruvá o lorito güí-güí”. Otros: Burgo cola recta, maracaná del suelo, papagayo de la barranca, tutú (de la Peña, 2020:24; Chébez, 1996:137).
En otros idiomas
Breves apuntes históricos:
- Apuntamientos para la Historia Natural de las Paxaros del Paraguay y Rio de la Plata. Azara, Félix de. Madrid, 1802-1805. Vol I: 243. (Tutu)
- Histoire naturelle des oiseaux de paradis et des rolliers : suivie de celle des toucans et des barbus. Le Vaillant, François. Paris: Chez Denné le jeune … [et] chez Perlet …, 1806. Vol I: 139; Ilustración 39. (Le Momot Dombé)
- Histoire naturelle des promerops, et des guêpiers: faisant suite à celle des oiseaux de paradis par la même. Le Vaillant, François. Paris: [publisher not identified], 1807: 41; figura B. (Le Momot Oranroux Male)
- Nouveau dictionnaire d’histoire naturelle, appliquée aux arts, à l’agriculture, à l’économie rurale et domestique, à la médecine, etc. Par une société de naturalistes et d’agriculteurs. Paris, Chez Deterville, 1816-19. Vol XXI (1818): 315. (Baryphonus ruficapillus)
- General zoology, or Systematic natural history. Shaw, George. London, Printed for G. Kearsley, 1800-1826. Vol XIV: 84. (Momot rubricapillus)
- La galerie des oiseaux. Vieillot, L. P., Last, Carel Christiaan Antony, lithographer, Marais, R. des, lithographer, Motte, Charles Etienne Pierre, lithographer, Oudart, P. L. Paris: Carpentier-Méricourt, 1834. Vol II (1825): 319; Ilustración 190. (Le momot Dombey – Baryphonus ruficapillus)
- Conspectus generum avium. Bonaparte, Charles Lucian. Lugduni Batavorum: Apud E.J. Brill, 1850-1857. Vol I (1850): 165. (Prionites ruficapillus)
- Catalogue of a collection of American birds. Sclater, Philip Lutley. London: N. Trubner and Co., 1862. pp: 262. (Baryphthengus ruficapillus)
- Catalogue of the birds in the British Museum. British Museum (Natural History). Department of Zoology. London, 1874-98; Vol 17: 330-331. (Baryphthengus ruficapillus)
- As aves do Estado de S. Paulo. Ihering, H. von (Hermann). S. Paulo :Typ. a vapor de Hennies irmãos,1898; pp: 291. (Baryphthengus ruficapillus)