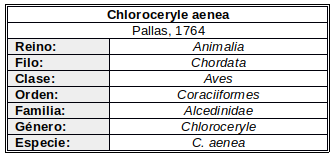
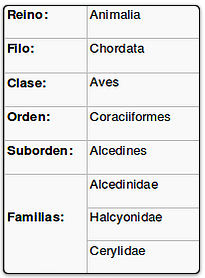
Órden Coraciiformes, 6 Familias (Meropidae, Coraciidae, Brachypteraciidae, Todidae, Momotidae y Alcedinidae) (del Hoyo, 2020:298).
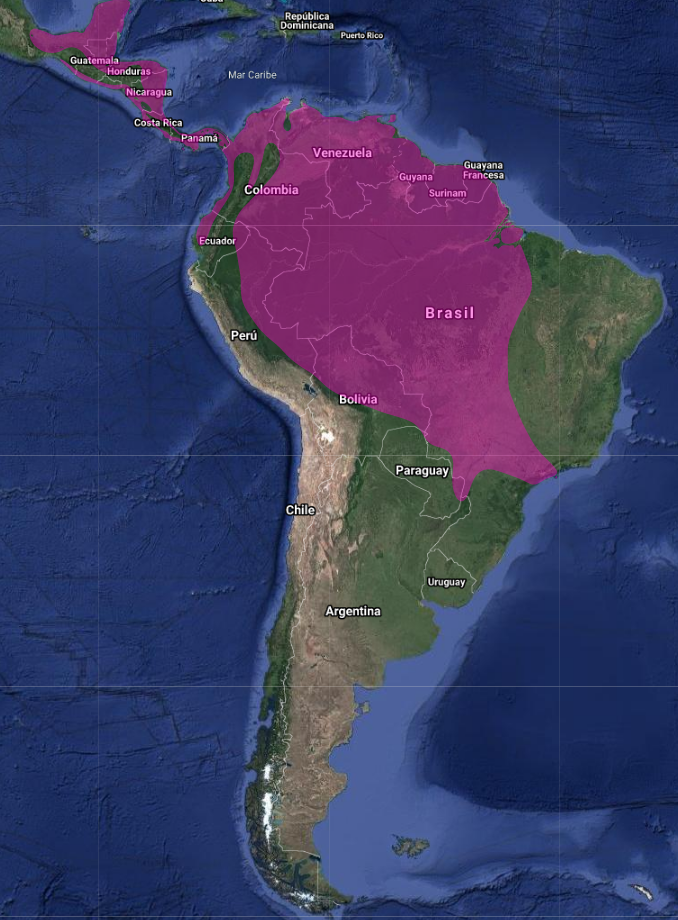
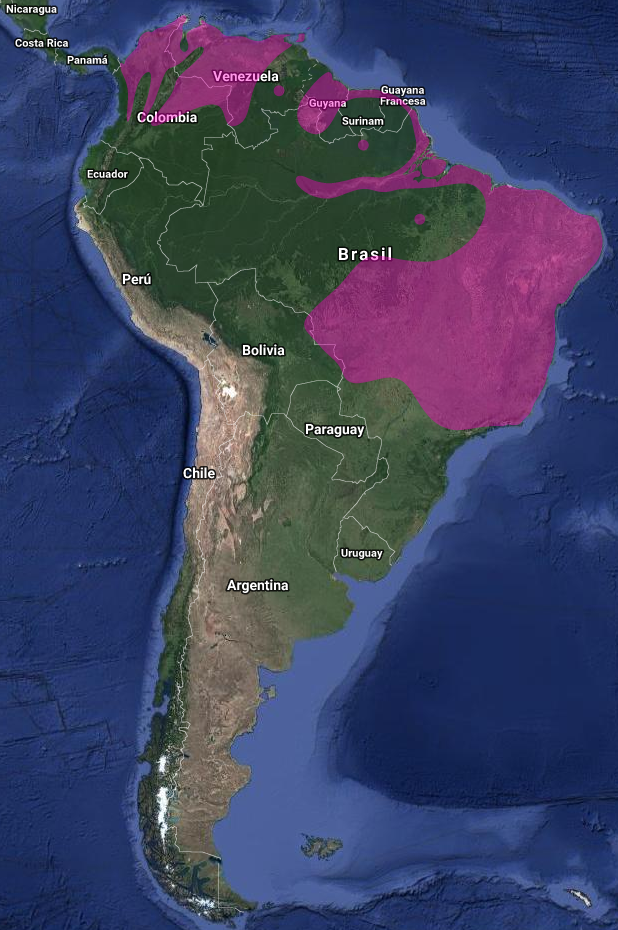
Los Martines Pescadores son de distribución mundial y en las Américas están representados pobremente, ya que de las 87 especies conocidas únicamente se encuentran 6 en el Nuevo Mundo (4 en Argentina, 4 en Misiones)
En Argentina, 2 Géneros y solo 4 especies, las cuatro se encuentran en Misiones:
- Familia Alcedinidae
- Género Megaceryle
- Género Chloroceryle
La taxonomía de las tres familias es compleja y bastante polémica. Aunque hay un consenso general en emplazarlo dentro del Orden Coraciiformes, de este nivel para abajo aparecen los conflictos.
El centro de mayor diversidad del grupo es la región de Australasia, pero no se originó allí. Evolucionaron en el hemisferio norte e invadieron Australasia varias veces. Se han encontrado alcedines fósiles en rocas procedentes del Eoceno inferior de Wyoming y del Eoceno medio en Alemania, hace unos 30-40 millones de años. Se han descrito fósiles más recientes procedentes de rocas del Mioceno en Australia (hace 5-25 millones de años). El escaso número de especies que se encuentran en América, todas ellas de la familia Cerylidae, sugiere que esta pequeña representación procede solo de dos especies colonizadoras. Esta familia sería una rama relativamente reciente bifurcada de Halcyonidae, que se diversificó en el Viejo Mundo, en épocas tan recientes como el Mioceno o el Plioceno. El grupo se había tratado tradicionalmente como una familia, Alcedinidae, con tres subfamilias, pero tras la revolución de los años 1990 en la taxonomía de las aves, las tres antiguas subfamilias ahora son frecuentemente elevadas al nivel de familias. Este traslado se sustentó en estudios cromosómicos y de hibridación ADN-ADN, pero planteaban el problema de que los tres grupos resultaban monofiléticos con respecto al resto de Coraciiformes. Esto condujo a agruparlas en el suborden Alcedines.
DESCRIPCIÓN
Al contrario que las especies del Viejo mundo, los Martines Pescadores neotropicales son de apariencia bastante homogénea, pero de tamaño mucho más diverso.
Al contrario que las especies del Viejo mundo, los neotropicales son de apariencia bastante homogénea, pero de tamaño mucho más diverso.
Este orden se caracteriza por la forma del paladar, los dedos y el pico.
De tamaño pequeño (entre 17-20 cm) incluyendo el pico de unos 4 cm). Cuerpo corto y rechoncho con cabeza relativamente grande con semicopete.
Plumaje denso y liso, vistoso, colorido y brillante (iridiscente), generalmente verdes o azules. Alas cortas, redondeadas. Aparentemente mueven las alas sobre el agua remando o utilizándolas como timón.
Pico proporcionalmente grande, recto, robusto,semejante a una lanza (el pico generalmente es más largo y estrecho en las especies que atrapan peces, y más corto y ancho en las que cazan presas por el suelo). Lengua corta
El iris de la mayoría de las especies es pardo oscuro. Tienen una excelente visión (binocular) y se cree que con una apreciación del color especialmente buena. Tienen el movimiento del ojo restringido dentro de la cavidad ocular; en su lugar mueven la cabeza para seguir a sus presas. Tiene 2 fóveas en los ojos, una para el campo monocular (la primera detección) y otra para el campo binocular (detección de precisión), que es excelente. Además son capaces de compensar la refracción del agua y el reflejo cuando atrapan presas bajo el agua, y son capaces de apreciar la profundidad con exactitud. También tienen membranas nictitantes para proteger los ojos del impacto con el agua.
Cola de tamaño medio, tarsos cortos, dedos pequeños: 3 dedos hacia delante, 2 de ellos unidos y 1 hacia atrás (sindáctiles). A la hora de excavar, los dedos delanteros (unidos en la base) les sirven como «pala»
No existe dimorfismo sexual excepto cuando crían, teniendo entonces el macho el pico negro y la hembra la parte inferior de la base del pico anaranjado o rojizo. Los jóvenes son similares al adulto, pero con el color más apagado y las patas grisáceas.
ALIMENTACIÓN
Se alimentan de invertebrados y pequeños vertebrados acuáticos, incluyendo peces.
Asentados sobre rama aislada cerca del agua, (con las plumas del cuello izadas, alas caídas, moviendo la cola ligeramente para arriba y abajo llegando a veces a colocarla verticalmente) observan la vida acuática zambulléndose para capturar peces o larvas e insectos que se encuentran a flor de agua. También cazan a pleno vuelo.
La focalización de la presa debajo del agua (difícil por la refracción del agua) es facilitada por la existencia de 2 fóveas, una central y otra lateral, que posibilitan una visión tanto monocular como binocular. Esta modalidad de pesca se ve dificultada en aguas turbias (después de grandes lluvias, por ejemplo) por lo que se tornan insectívoros o emigran.
Los miembros de las tres familias golpean a las presas grandes contra el posadero hasta matarlas, o bien para quitar o romper sus espinas y caparazones. Una vez golpeada la presa se la colocan para poder tragarla.
COMPORTAMIENTO
Monógamos , solitarios y pasivos. Principalmente arborícolas. Territoriales, defienden su territorio agresivamente. Postura vertical. Se zambullen para capturar peces.
Vuelo rápido y ondulado.
VOCALIZACIONES: Llamada de alarma semejante a «chasquidos» pudiendo terminar como un estridente «matraqueo». Los «Chloroceryle amazona y Chloroceryle americana» emiten un canto melodioso.
HÁBITAT
Vive en arroyos, ríos, embalses, esteros, pantanos, lagunas y zonas costeras. Generalmente aparece a poca altitud, por debajo de los 1.000 m s.n.m, aunque puede aparecer en zonas de montaña, si las condiciones son favorables.
REPRODUCCIÓN
Monógamos. Anidan en cavidades que excavan en barrancas arenosas en orillas de ríos y lagos. El excavado del nido es compartido por ambos miembros de la pareja. Huevos blancos, brillantes. La puesta suele ser de 4-6 huevos, dos veces al año. Comparten la incubación durante 3 semanas aproximadamente. Nacen desnudos y permanecen en el nido 4 semanas.
BIBLIOGRAFÍA
- A Classification of the Bird Species of South America. South American Classification Committee. American Ornithologists’ Union (Parte V)
- Ares R. (2007) Aves: vida y conducta. 1º ed. Vázquez Mazzini Editors, Buenos Aires: 61
- Azara, Félix de (1802-1805). Apuntamientos para la historia natural de las Paxaros del Paraguay y Rio de la Plata; Vol II: 380-383 (enlace)
- Cebolla Badie M. (2000) El conocimiento mbya-guaraní de las aves. Nomenclatura y clasificación. Suplemento Antropológico; Vol XXXV, n.º 2: 9-188 (enlace)
- De la Peña M.R. (1987) Nidos y huevos de Aves Argentinas: 101
- De la Peña M.R.; F.C.; Laene Silva, R.; Capuccio, G. y Bonin, L.M (2009) Aves del Río Uruguay, Guía Ilustrada de Especies del Bajo uruguay y el Embalse de Salto Grande. Comisión Administradora del Río Uruguay. CARU: 124
- De la Peña M.R. (2015). Aves argentinas. Eudeba (Ed. UNLP); Vol 1: 367
- Enciclopedia Británica (1998); Vol 15; Macropedia: Birds: 89
- Moroney, M. K., & Pettigrew, J. D. (1987). Some observations on the visual optics of kingfishers (Aves, Coraciformes, Alcedinidae). Journal of Comparative Physiology A, 160(2), 137-149. (enlace)
- Moyle, R. G. (2006). A molecular phylogeny of kingfishers (Alcedinidae) with insights into early biogeographic history. The Auk, 123(2), 487-499. (enlace)
- Narosky T., Yzurieta D.(2010) Guía de identificación de aves de Argentina y Uruguay. Ed. Vázquez Mazzini: 42 y 210
- Olrog, C.Ch. (1959). Las Aves Argentinas. Una Guía de Campo. Universidad Nacional de Tucumán. Instituto Miguel Lillo. Argentina; 167
- Sharpe, Richard Bowdler (1868-71.) A monograph of the Alcedinidae : or, family of kingfishers. . London: Published by the author
- Sick Helmut (1997). Ornitologia Brasileira. Editora Nova Fronteira, Río de Janeiro: 472-475
- Woodall, P.F. (2017). Kingfishers (Alcedinidae). In: del Hoyo, J., Elliott, A., Sargatal, J., Christie, D.A. & de Juana, E. (eds.). Handbook of the Birds of the World Alive. Lynx Edicions, Barcelona. (retrieved from on 11 July 2017).