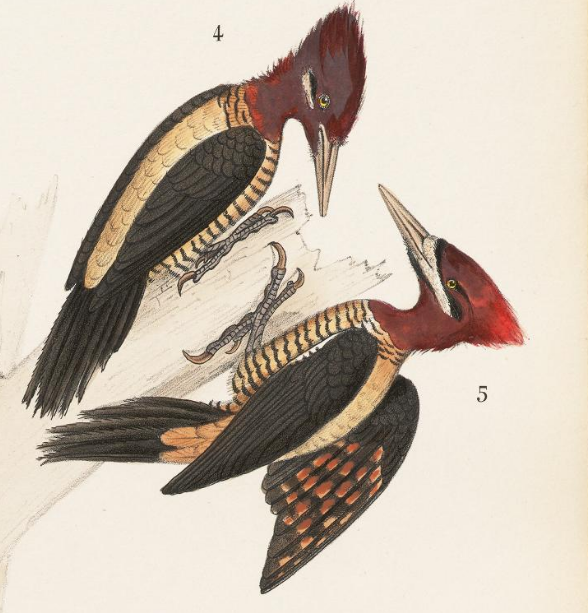
NOMBRE COMUNES
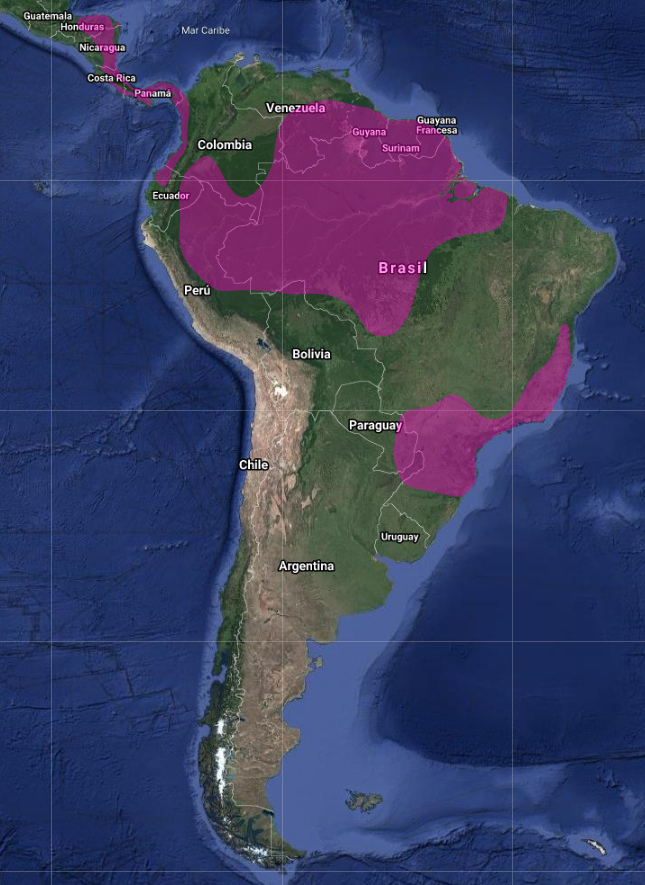
Carpintero grande, Carpintero listado de garganta roja; Carpintero gigante, Carpintero listado grande (Argentina, Paraguay) (De la Peña, 2016:105); Picamaderos robusto, Pito listado grande; En Brasil, Pica-Pau Grande, Pica-pau-de-cabeça-vermelha, Pica-pau-galo, Pica-pau-rei, Pica-pau-soldado, Pinica-pau. En guaraní “Ipekú” “Ypekû guasu ka’aguy” (Chébez, 1996)
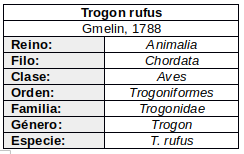
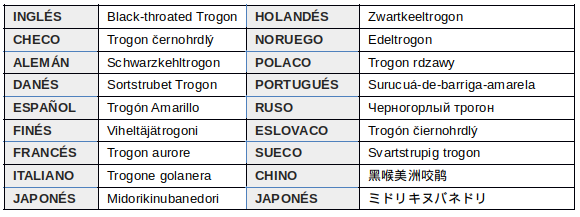
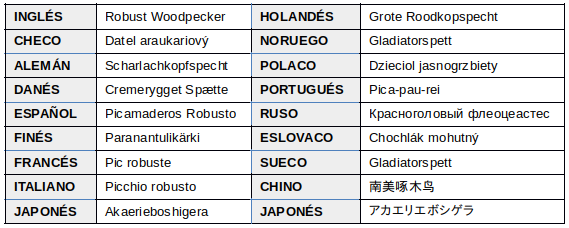
EN OTROS IDIOMAS
NOTAS ANTROPOLÓGICAS
* La Dra. Badie, en “El conocimiento mbya-guaraní de las aves. Nomenclatura y clasificación” (2000) comenta sobre el Carpintero cabeza colorada (Campephilus robustus), o Ipekû akâ pŷta ó pŷta: Según explicó el Pa’i de Jejy cuando este pájaro carpintero emite sus cantos sobre la casa de una persona le está anunciando la llegada de visitas en un tiempo aproximado de uno o dos días, de esta forma, atendiendo al canto del carpintero la familia puede ir haciendo los preparativos para esperarlas. Esta especie también recibe el nombre de poi poi, porque cuando anuncia noticias canta emitiendo estas palabras “A dice poi poi, eso es que trae noticias, a la tardecita va a venir alguien, algún hombre está por dejar a su mujer o alguna persona va a morir, todo eso puede anunciar” (Manuel de Takuapí), en Cebolla Badie, 2000:60)
BREVES APUNTES HISTÓRICOS
- Apuntamientos para la historia natural de los páxaros del Paragüay y Rio de la plata. Félix de Azara. Imprenta Viuda de Ibarra (1805) Tomo 2: 301-303 (Carpintero gorro y cuello roxos) (enlace)
- Zur Ornithologie Brasiliens : Resultate von Johann Natterers Reisen in den Jahren 1817 bis 1835. Pelzeln, August von, Natterer, Johann. Wien :A. Pichler’s Witwe & Sohn,1871: 243 (Campephilus robustus)
- Traité d’ornithologie, ou, Tableau méthodique des ordres, sous-ordres, familles, tribus, genres, sous-genres et races d’oiseaux : ouvrage entièrement neuf, formant le catalogue le plus complet des espèces réunies dans les collections publiques de la France. Lesson, R. P. (René Primevère), Prêtre, J. G., ill. Bruxelles: Chez F.G. Levrault ;1831; Tomo I: 225 (Picus robustus)
- Avium species novae, quas in itinere annis MDCCCXVII-MDCCCXX per Brasiliam. Spix, Johann Baptist von, Martius, Karl Friedrich Philipp von, Schmidt, Matthias, ill. Monachii: Impensis editores,1838-1839; Pág. 56; ilustración XLIV (Picus robustus)
- The genera of birds : comprising their generic characters, a notice of the habits of each genus, and an extensive list of species referred to their several genera. Gray, George Robert, Hullmandel, Charles Joseph, Mitchel David W., Hullmandel y Walton, printer of plates. London: Longman, Brown, Green, and Longmans,1849; Vol 2: 436. (Campephilus robustus)
- Conspectus generum avium. Bonaparte, Charles Lucian. Lugduni Batavorum :Apud E.J. Brill,1850-1857; Tomo 1 (1850): 133
- Monographie des picidées, ou Histoire naturelle des picidés, picumninés, yuncinés ou torcols; comprenant dans la première partie, l’origine mythologique, les mœurs, les migrations, l’anatomie, la physiologie, la répartition géographique, les divers. Malherbe, Alfred. Metz,Typ. de J. Verronnais,1861-62; Tomo I (1861): 23; Tomo III (1861): ilustración III (fig. 4 y 5) (Megapicus robustus)
- Catalogue of a collection of American birds. Sclater, Philip Lutley. London: N. Trubner and Co.,1862: 332 (Campephilus robustus)
- Catalogue of the birds in the British Museum. British Museum (Natural History). Department of Zoology. London, 1874-98; Vol 18 : 477-478
- As aves do Brasil. Series: Monographias Brasileiras. Göldi, Emil August. Rio de Janeiro [etc.] :Alves & c.,1894-[1900]: 149
- Iconographia Zoologica – Special Collections University of Amsterdam Lámina DCLI (Campephilus robustus)