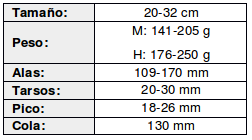
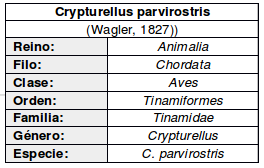
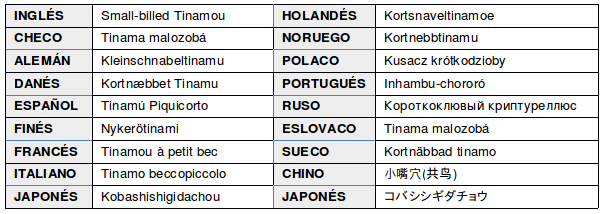
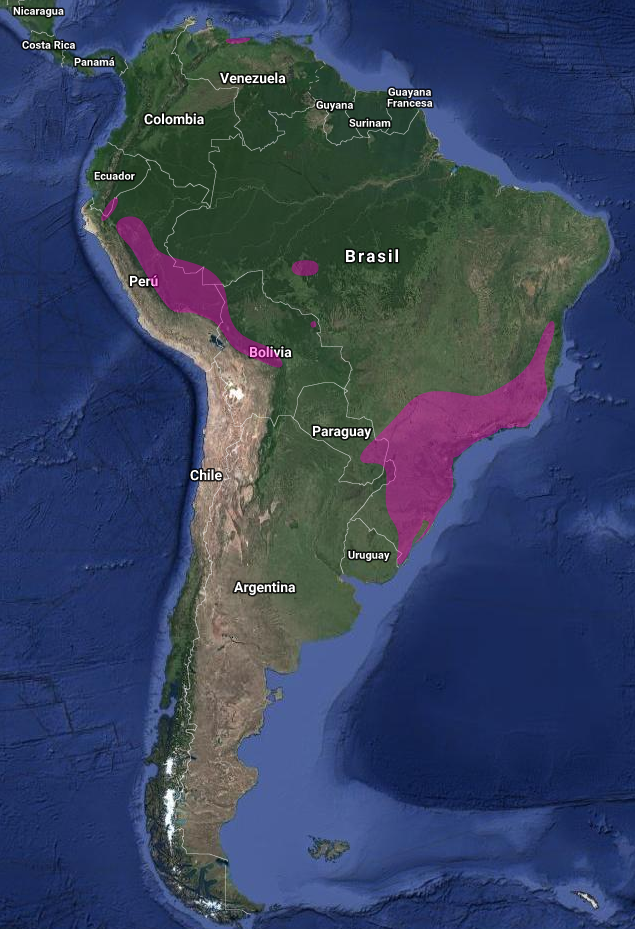
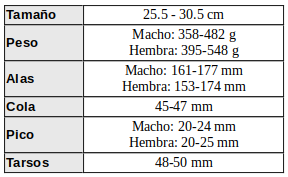
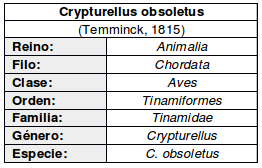
Las aves del género Crypturellus, incluyendo al Tataupá rojizo (Crypturellus obsoletus), presentan características típicas de las aves gallináceas. Son animales principalmente terrestres, con habilidades de vuelo limitadas, realizando desplazamientos cortos y preferentemente permaneciendo en el suelo (Sick, 1997:154; Alborghetti, 208:8).
Estas aves son sedentarias y difíciles de avistar (Hilty, 2003:182-183). Mantienen hábitos solitarios, salvo durante la temporada de reproducción (Handford & Mares, 1985; Belton, 1984:400; Alborghetti, 2018:8). Son especialistas en explorar los estratos inferiores del bosque y rara vez abandonan esta zona (Alborghetti, 2018:8; Chebez, 1990:21-22; Gomes, 2020). Utilizan senderos en su hábitat, corriendo entre los matorrales con el cuello extendido y los tarsos algo doblados. Además, suelen defender territorios pequeños, mostrando comportamientos agresivos entre sí (Estevo et al., 2017:11; Alborghetti, 2018:8).
Durante ciertos momentos del día, emiten silbidos que suelen ser más audibles por la mañana o al atardecer, especialmente al dirigirse al lugar de descanso y al llamar a sus parejas (Pereyra, 1950:178). Se estima que para sostener dos o tres pares de Tataupá rojizos se requieren al menos 20 hectáreas de hábitat adecuado (Magalhães, 1994:17; Gomes, 2020).
En cuanto a su sistema reproductivo, se observa que sigue una dinámica de poliginia simultánea para los machos y poliandria secuencial para las hembras, un patrón común entre los tinamúes y especies afines (Cabot, 1992:119).
VOCALIZACIONES
Los tinamúes carecen de aprendizaje vocal, como se ha afirmado por Hardy et al. (1993) y Gomes (2020). Sus canciones son innatas y no se ven influenciadas por la experiencia o el aprendizaje. Esta canción innata se desarrolla sin una plantilla preexistente y está determinada genéticamente (Gomes, 2020). Sin embargo, se han observado variaciones geográficas en los cantos de los tinamúes, lo que sugiere que la selección natural puede favorecer diferentes estructuras de canto en distintos hábitats (Bertelli & Tubaro, 2002:429; Alborghetti, 2018:8 y 14; Laverde & Cadena, 2014:490; Vieillard, 1987:148; Vieillard, 2004:148).
La voz es grave, lo que les permite adaptarse al entorno del estrato inferior del ambiente forestal, donde abundan troncos y ondulaciones del terreno. Esta característica les otorga un mayor alcance que los sonidos agudos. (Sick, 1997:155).
Sick (1997:163) describe las vocalizaciones de los tinamúes como un silbido fuerte que se asemeja al silbato de un guarda de tráfico, o como una estrofa compuesta que comienza de manera pausada y se acelera a medida que asciende, terminando en un tono más grave. Además, menciona una serie simple y vibrante de trinos ascendentes relativamente cortos, sin pausas prolongadas, que también terminan en un tono más grave.
En cuanto a las diferencias entre las vocalizaciones de machos y hembras, se señala que los machos emiten un pío fortísimo seguido de una secuencia ascendente relativamente corta, mientras que las hembras emiten una secuencia ascendente extremadamente prolongada, con pausas acentuadas al inicio y aceleradas al final, volviéndose muy fuerte. Además, las hembras emiten secuencias ascendentes cortas de píos fuertes e iguales, así como secuencias irregulares de píos suaves y débiles, que funcionan como lloros para llamar al macho.
El autor también hace referencia a la distinción entre vocalizaciones simples y complejas: las simples constan de unas pocas notas del mismo tipo y se denominan llamadas, mientras que los cantos son más complejos, con más de tres notas, a menudo de diferentes tipos (Sick, 1997:163; AlborgHetti, 2018:8).
La descripción de la canción es detallada por Schulenberg et al. (207:32), quienes la definen como una larga serie de frases sonoras que aumentan de tono y aceleran en ritmo hasta cerca del final. Al finalizar, la voz «se quiebra» y las notas se transforman en silbidos más limpios, como «Prr… prr… prr prr prr, prr, prr-prr-prr-prr’prr’pi’pi’pi?». Por otro lado, la llamada diurna, similar en calidad a una canción, es una frase más corta de notas ascendentes, como «Prrrr, prr-prree?».
Varios autores, como Chebez (2015:23), Straneck (1992:2), Chebez (1990:21-22), y de la Peña (2020:28-30), describen las vocalizaciones como una sucesión de potentes ritmos ascendentes en modulaciones de frecuencia, acelerándose hacia el final hasta hacerse inaudibles, representadas por sonidos como «Frü… Frü… Frü… Friü…Frií….Fríh… Fríh…Fíh…Fhh…». En Argentina, estas vocalizaciones son más frecuentes durante la primavera hasta el mes de diciembre, especialmente al atardecer y después de las lluvias.
ALIMENTACIÓN
La dieta de los tinamúes, aunque poco conocida, incluye una variedad de elementos vegetales y, ocasionalmente, invertebrados. Se ha observado que consumen semillas de frutos silvestres, granos y fragmentos vegetales que obtienen generalmente del suelo o de las plantas a su alcance. Ocasionalmente, pueden saltar para alcanzar un fruto o insecto (Cabot, 1992:118; Alborghetti, 208:8).
Se han registrado diferentes tipos de frutos y semillas consumidos por los tinamúes, provenientes de familias como Lauraceae, Euphorbiaceae (incluyendo frutos de Mabea fistulifera), Rutaceae, Musaceae (Heliconia), Rubiaceae, Marantaceae, y Poaceae (Guadua superba) (Moojen, 1941:406; Gomes, 2020; Cabot, 1992:129; Vieira et al., 1992:66). Además, consumen insectos como coleópteros (Curculionidae), ortópteros, larvas de lepidópteros, y siguen a las hormigas legionarias (Formicidae) para capturar los insectos que huyen de ellas.
Se presume que los tinamúes consumen regularmente invertebrados. Willis (1983) observó a un par de tinamúes pardos siguiendo un enjambre de hormigas armadas (Labidus praedator), cerca de las cuales «picoteaban presas diminutas de vez en cuando». Esto sugiere que los tinamúes complementan su dieta vegetal con la ingesta ocasional de invertebrados que encuentran en su entorno (Cabot, 1992:118; Alborghetti, 208:8).
REPRODUCCIÓN
La información sobre la biología reproductiva de los tinamúes es limitada pero interesante. Según Cabot (1992:120), la incubación y el cuidado de las crías son responsabilidades exclusivas de los machos. Sin embargo, Sick (1993:98) reportó una observación excepcional de una hembra con dos crías, lo que podría indicar una situación inusual donde la hembra asumió el rol del progenitor masculino faltante.
Se destaca que las hembras tienen un papel importante en la definición y mantenimiento de los territorios, así como en el proceso de atracción y competencia por los machos reproductores (Magalhães, 1994:17; Alborghetti, 2018:8).
Anidan en depresiones en el suelo, generalmente al pie de un árbol. La puesta consta típicamente de 3-4 huevos, los cuales pueden tener un color rosa intenso o marrón chocolate, dependiendo de la región (Frisch & Frisch, 1964, citado en Gomes 2020). La incubación dura alrededor de 19 días en cautiverio (Cabot, 1992:129).
En Argentina, se han localizado nidos de tinamúes en la provincia de Misiones, con posturas que varían entre 4-5 y 5-7 huevos, observadas principalmente entre los meses de agosto y noviembre (Chebez, 1990:21-22; Chebez, 2015:23; Hartet & Venturi, 1909:264; de la Peña, 2020:28-30).
En resumen, los tinamúes presentan una biología reproductiva intrigante y diversa, con una distribución de roles entre machos y hembras y adaptaciones particulares en el proceso de nidificación y cuidado de las crías.